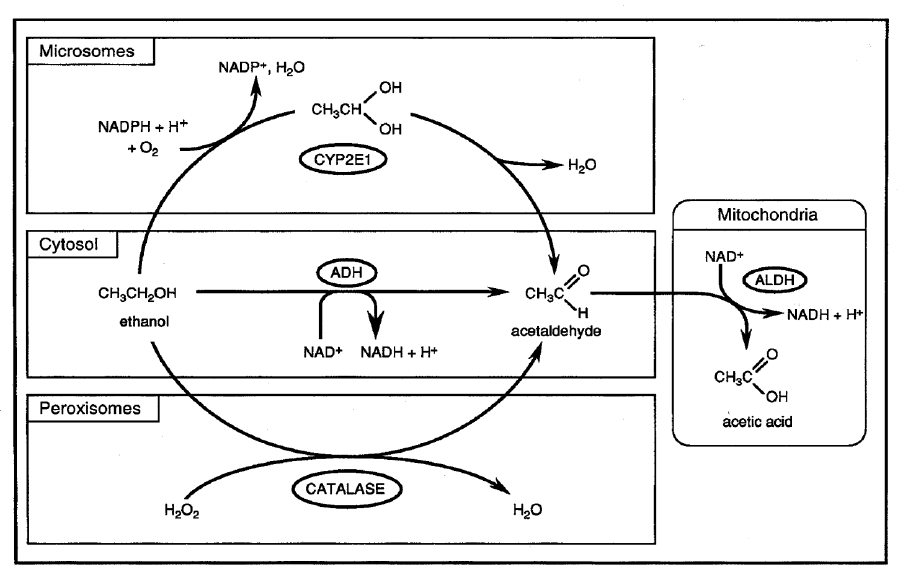
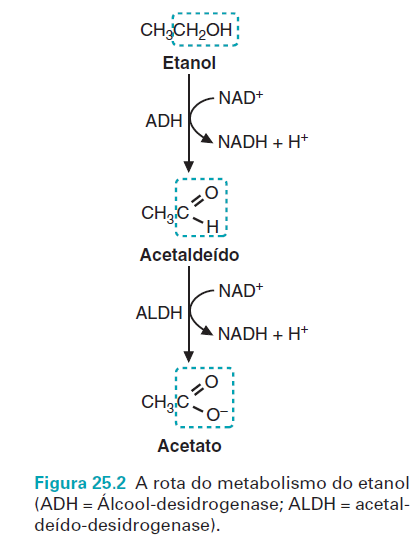
Ometabolismo ocorre em três etapas: oxidação do etanol em a cetaldeído, oxidação acetaldeído em aldeído, e oxidação do aldeído em acetil-CoA.
O etanol é uma molécula pequena, com absorção relativamente lenta pelo estômago e absorção mais rápida pelo intestino. Por ser solúvel em água, ele acessa rapidamente a corrente sanguínea por difusão passiva – de onde é livremente distribuído para a maioria dos órgãos e sistemas.
uma pequena parte do etanol ingerido (0 a 5%) entra na mucosa gástricas de células do trato gastro intestinal alto e o restante passa para o sangue. Desses 85 a 95% são metabolizados no fígado e somente 2 a 10% são excretados pelos pulmões e rins.
O álcool é uma fonte de energia dietética metabolizado a acetato principalmente no fígado através de uma série de alterações metabólicas de reações oxidativas.

Ometabolismo ocorre em três etapas: oxidação do etanol em a cetaldeído, oxidação acetaldeído em aldeído, e oxidação do aldeído em acetil-CoA.
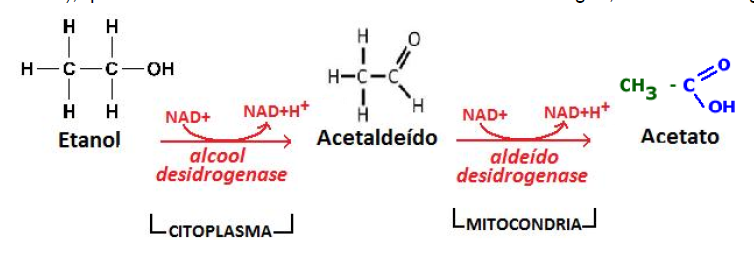


A principal rota de metabolização do etanol é através da álcool desidrogenase (ADH) hepática pela oxidação do álcool a acetaldeído. Isso ocorre no citosol.
Nessa primeira fase, há formação de acetaldeído pelo sistema ADH, sendo consumido NAD+ e produzido NADH + H+, sua forma reduzida.
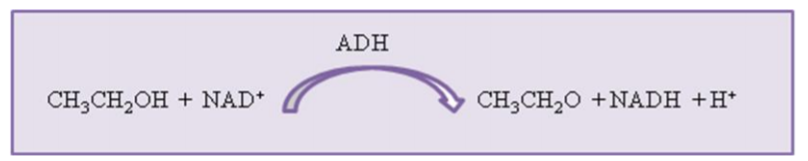


Assim, na oxidação do etanol pela ADH ocorre a formação de um mol de NADH para cada mol de etanol oxidado.
OBS: Se não for removida por metabolismo, o acetaldeído exerce efeito tóxico no fígado, passar para o sangue e causar efeitos tóxicos em outros órgãos e tecidos. O acetaldeído é altamente reativo. Ele se liga covalentemente a grupos aminos, grupos sulfidrilas, nucleotídeos e fosfolipídios para formar “aductos”.
OBS: Cerca de 90% do acetaldeído produzido é posteriormente metabolizado em acetato no fígado pela enzima acetaldeído desidrogenase (ALDH).
A ADH é uma família de isoenzimas com variação específica no comprimento da cadeia do substrato do álcool e, estando o etanol em grande concentração, é metabolizado de forma não específica por muitos membros da família ADH. As álcool-desidrogenases que apresentam maior especificidade pelo etanol são da classe álcool-desidrogenase I.
A classe I de álcool-desidrogenases está presente em altas quantidades no fígado, representando cerca de 3% do total de proteína solúvel. Essas álcool-desidrogenases, em geral referidas coletivamente como álcool-desidrogenase hepática, apresentam um Km baixo para etanol entre 00,5 a 4 mM (altas afinidades). Portanto, o fígado é o principal sítio de metabolização do álcool e de formação do metabólito tóxico (acetaldeído).
Existem também, enzimas das classes IV e II apresentem uma menor contribuição para o metabolismo do etanol. Elas podem contribuir para o seu efeito tóxico. Os genes ADH de classe II são primeiramente expressos no fígado e, em níveis mais baixos, no trato gastrintestinal inferior.
Existem relatos de que a ADH pode participar em numerosas outras reações, sendo portanto considerada uma enzima bastante inespecífica, uma vez que pode catalizar a interconversão de um grande grupo de álcoois primários e secundários e os seus respetivos aldeídos e cetonas, existindo também em tecidos extra-hepáticos, tais como o estômagos e o intestino, tendo um efeito na absorção e biodisponibilidade do etanol.
A aldeído desidrogenase (ALDH) é responsável pela oxidação do acetaldeído —> acetato. Esta reação está associada com o elevado fornecimento energético proveniente do NADH na formação de 16ATP/mol (Trifosfato de adenosina – ATP) de etanol.
Mais de 80% da oxidação de acetaldeído no fígado humano é normalmente catalisada por acetaldeído-desidrogenase mitocondrial (ALDH2), que apresenta uma alta afinidade por acetaldeído e é altamente específica. A maior parte da oxidação do acetaldeído restante ocorre por meio de uma acetaldeído-desidrogenase citosólica (ALDH1). Acetaldeído-desidrogenases adicionais agem em uma variedade de alcoóis orgânicos, toxinas e poluentes.
O metabolismo do acetato requer a ativação de acetil-CoA pela acetil-Coa-sintetase em reação similar à catalisada por acetil-CoA-sintetase graxa. No fígado, a principal isoforma da acetil-CoA-sintetase (ACS I) é uma enzima citosólica que forma acetil-CoA pela rota citosólica da síntese de colesterol e ácidos graxos. A entrada de acetato nessa rota está sob controle regulatório de mecanismos envolvendo colesterol e insulina. Portanto, a maior parte de acetato formado passa para o sangue. O acetato é captado e oxidado por outros tecidos, principalmente coração e músculo esquelético, os quais têm uma alta concentração mitocontrial da isoforma de acetil-CoA-sintetase (ACS II). Essa enzima está presente na matriz mitocondrial e, por isso, forma acetil-CoA, que pode entrar diretamente no ciclo TCA e ser oxidada a CO2.


Há diferentes isoformas de ADH e ALDH, codificadas por diferentes genes, o que determina uma variabilidade étnica e individual na capacidade de degradação do álcool, ocorrendo, em alguns indivíduos, o acúmulo de acetaldeído a partir da ingestão de quantidades relativamente pequenas de álcool
OBS: Em indivíduos portadores da ADH3 (alelo da rápida metabolização do álcool) apresentam um risco aumentado de desenvolvimento de cancro de boca, quando comparados com os indivíduos portadores da ADH1
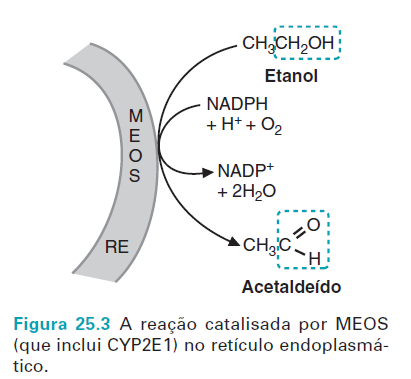
OBS: MEOS que demostrou não só a sua existência mas sobretudo a sua participação na destruição de 20% do álcool ingerido num modelo de consumo excessivo, cuja diferença está, na sua sensibilidade ao dióxido de carbono e na maior afinidade ao etanol


OBS: O acúmulo de acetaldeído causa náusea e vômito, e, dessa forma, a acetaldeído-desidrogenase inativa é relacionada aos comportamentos desagradáveis provocados pelo álcool e protege contra o alcoolismo.
MEOS é parte da superfamília de enzimas do citocromo P450 (é uma isozima oxidase), as quais catalisam reações oxidativas similares. O gene citocromo P4502E1 (CYP2E1) codifica uma enzima que é a principal constituinte do Sistema microssomal de oxidação do etanol. Variações genéticas presentes no gene CYP2E1 resultam em diferenças significativas na atividade enzimática, entretanto o significado funcional dessas variações no metabolismo do etanol permanece controverso, uma vez que ainda não existe uma correlação evidente com diferenças na atividade catalítica da enzima. Porém, sabe-se que a CYP2E1 apresenta maior atividade para o etanol.
OBS: A CYP2E1 tem um Km muito maior para o etanol do que a classe I das álcool-desidrogenases
OBS: Em altos níveis de álcool no organismo, o etanol será mais metabolizado pela CYP2E1 do que em baixos níveis.
O consumo crônico de etanol aumenta os níveis hepáticos de CYP2E1 cerca de 5 a 10 vezes e causa, também, um aumento de duas a quatro vezes em algumas das outras P450 da mesma família, de diferentes subfamílias e até mesmo de diferentes famílias de genes. O retículo endoplasmático sofre proliferação, com um aumento geral no conteúdo das enzimas microssomais, incluindo aquelas que não são diretamente envolvidas no metabolismo do etanol.
OBS: MEOS se refere a atividade de oxidação do etanol combinada por todas as enzimas do P450.
OBS: O aumento na CYP2E1 com o consumo de etanol ocorre por meio de regulação de transcrição, pós-transcrição e pós- translação. Níveis aumentados de mRNA, resultantes da indução de transcrição do gene ou estabilização da mensagem, são encontrados em pacientes que consomem álcool com freqüência.
OBS: A especificidade sobreposta na atividade catalítica de enzimas P450 e nas suas induções é responsável por várias interações medicamentosas
OBS: O etanol é um inibidor da oxidação do fenobarbital pelo sistema P450. Quando grandes quantidades de etanol são consumidas, a inativação do fenobarbital é direta ou indiretamente inibida.
As enzimas do citocromo P450 são capazes de formar radicais livres, que também podem levar ao aumento de danos hepáticos e cirrose.
HISTÓRICO DE BEBIDA – O nível de álcool-desidrogenase gástrica (ADH) diminui e a CYP2E1 aumenta com uma prograssão de um singeloa um moderado e, em seguida, um pesado e crônico consumidor de álcool.
SEXO – Os níveis sanguíneos de álcool após o consumo de uma bebida são normalmente maiores nas mulheres do que nos homens, em particular devido aos baixos níveis de atividade de ADH gástrica nas mulheres. Após consumo crônico de etanol, a ADH gástrica diminui tanto nas mulheres quanto nos homens , mas as diferenças entre os sexos tornam-se ainda maior.
A diferença sexual nos níveis sanguíneos de álcool também pode ocorrer porque as mulheres em geral são menores. Dessa forma, no sexo feminino, o álcool é distribuído em um espaço 12% menor de água, porque a composição corporal das mulheres consiste em mais gordura e menos água do que a dos homens.
QUANTIDADE – Pequenas quantidades de etanol são metabolizadas mais eficientemente através de rotas de baixo Km de classe I ADH e classe II ALDH, e uma pequena acumulação de NADH ocorre para inibir o metabolismo do etanol via essas desidrogenases
Doenças induzidas pelo álcool, uma conseqüência comum e algumas vezes fatal do consumo abusivo, podem se apresentar em três formas: fígado gordo, hepatite induzida por álcool e cirrose. Cada uma pode ocorrer sozinha ou se apresentar em diversas combinações em um determinado paciente. A cirrose induzida por álcool é diagnosticada em 9% de todas as necropsias realizadas nos Estados Unidos, com um pico de incidência em pacientes com idade de 40 a 55 anos. Entretanto, a ingestão de etanol tem também efeito agudo no metabolismo hepático, incluindo inibição da oxidação de ácidos graxos e estímulo da síntese de triacilglicerol, levando, dessa foram, a um fígado gorduroso. Isso também pode resultar em cetoacidose ou acidose láctica e causar hipoglicemia ou hiperglicemia, dependendo do estado dietético. Esses efeitos são considerados reversíveis.
Em contraste, o acetaldeído e os radicais livres formados a partir do metabolismo do etanol podem resultar em hepatites induzidas por álcool, uma condição em que o fígado está inflamado, e as células se tornam necróticas e morrem. Danos difusos aos hepatócitos resultam em cirrose, caracterizada por fibrose (cicatrizante), alteração na arquitetura normal e fluxo sanguíneo, perda da função hepática e, por fim, insuficiência hepática.
As mais importantes repercussões metabólicas, decorrem do excesso da alteração no processo de oxidação-redução com modificação da relação NAD+/NADH, observando-se excesso de NADH, que como consequência há o comprometimento do metabolismo os carboidratos.
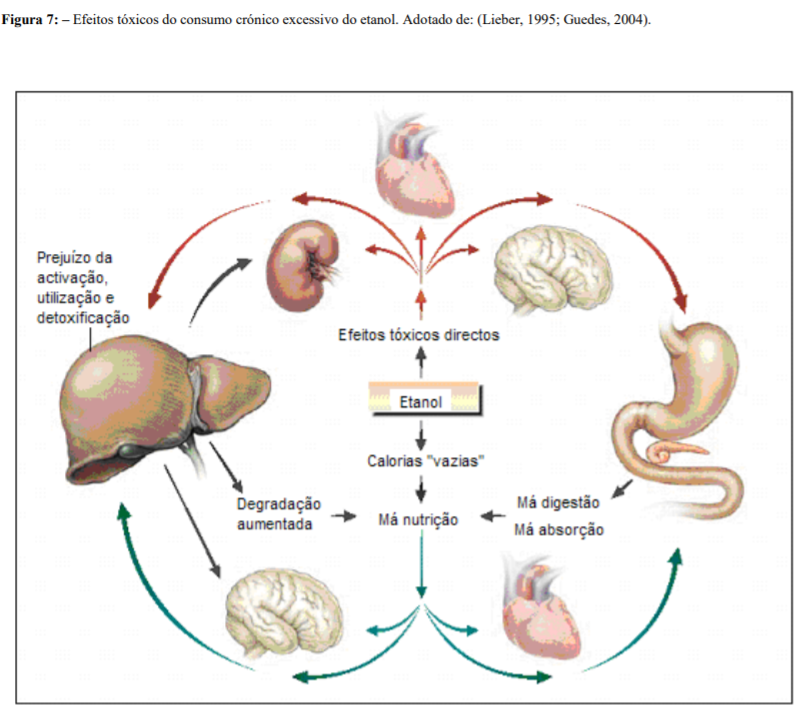


Um aspeto importante diz respeito à desestruturação no sistema de canais (microtúbulos) intracelulares que transportam as proteínas hepáticas para fora da célula levando à retenção hepática das chamadas “proteínas de exportação”, com consequente aumento do volume dos hepatócitos que vão levar a hepatomegalia. Ainda se observa a deformação e disfunção mitocondrial que, por sua vez, é geradora de um acumulo de aldeído acético, ácidos gordos e diminuição na função mitocondrial, que pode levar à necrose hepatocitária.
No tocante ao metabolismo das lipoproteínas traduz-se pelo desenvolvimento de hipertrigliceridemia. Neste sentido, o hepatócito desempenha um papel extremamente importante no processo de exportação de triglicerídeos, sob a forma de lipoproteínas de muito baixa densidade, que são formadas no REL e secretadas pelo complexo de Golgi e, dessa forma, a hipertrigliceridemia induzida pelo etanol representa, possivelmente, o aumento da síntese, secreção e retenção de lipoproteínas ricas em triglicerídeos no fígado que é responsável pelo desenvolvimento de esteatose hepática
O aumento do estresse oxidativo no fígado durante a intoxicação crônica por etanol surge do aumento da produção de radicais livres, principalmente pela CYP2E1. FAD e FMN na redutase e heme no sistema citocromo P450 transferem elétrons desemparelhados (singlet), operando, portanto, em mecanismos que podem formar radicais livres. O radical hidroxietil (CH3CH2O) é produzido durante o metabolismo do etanol e pode ser liberado como um radical livre. A indução da CYP2E1, assim como de outras enzimas do citocromo P450, pode aumentar a formação de radicais livres a partir do metabolismo de drogas e da ativação de toxina e carcinogênios (ver Figura 25.7, círculo 3). Esses efeitos são realçados pelos danos de aductos de acetaldeído.
O fosfolipídeo, o principal lipídeo da membrana celular, é um alvo primário de peroxidação causada pela liberação de radicais livres. A peroxidação de lipídeos no interior da membrana mitocondrial pode contribuir para a inibição de transporte de elétrons e no desacoplamento da mitocôndria, levando à inflamação e necrose celular.
A indução da CYP2E1 e de outros citocromos P450 também aumenta a formação de outros radicais e a ativação de hepatocarcinogenes.
A formação de aductos de acetaldeído realça os danos por radicais livres. O acetaldeído liga-se diretamente à glutationa e diminui sua habilidade em proteger contra H2O2 e prevenir a peroxidação lipídica, além de se ligar a enzimas de defesa de radicais livres.
Os danos à mitocôndria por acetaldeído e radicais livres perpetuam um ciclo de toxicidade. Com o consumo crônico de etanol, a mitocôndria começa a ficar danificada, a taxa de transporte de elétrons é inibida, e a fosforilação oxidativa tende a se tornar desacoplada. A oxidação de ácido graxo é diminuída o máximo possível, acentuando, dessa forma, a acumulação de lipídeos.






MARKS, C. S.; ALLAN D.; LIEBERMAN, M. Bioquímica Médica Básica de Marks: uma Abordagem Clínica, 2ª edição, Porto Alegre: Artmed, 2007
https://bdigital.ufp.pt/bitstream/10284/3757/1/Joana%20Vieira.pdf
http://bdtd.ibict.br/vufind/Record/PUC_GO_62724dc9aaa4f5bcb63c41f1a645f642
file:///C:/Users/draju/Downloads/bioqumicaii13-metabolismodoetanolarlindonetto-120627022300-phpapp02%20(1).pdf
IMAGEM: http://bioquimicadoalcool.blogspot.com/2012/06/diversidade-de-enzimas-que-participam.html