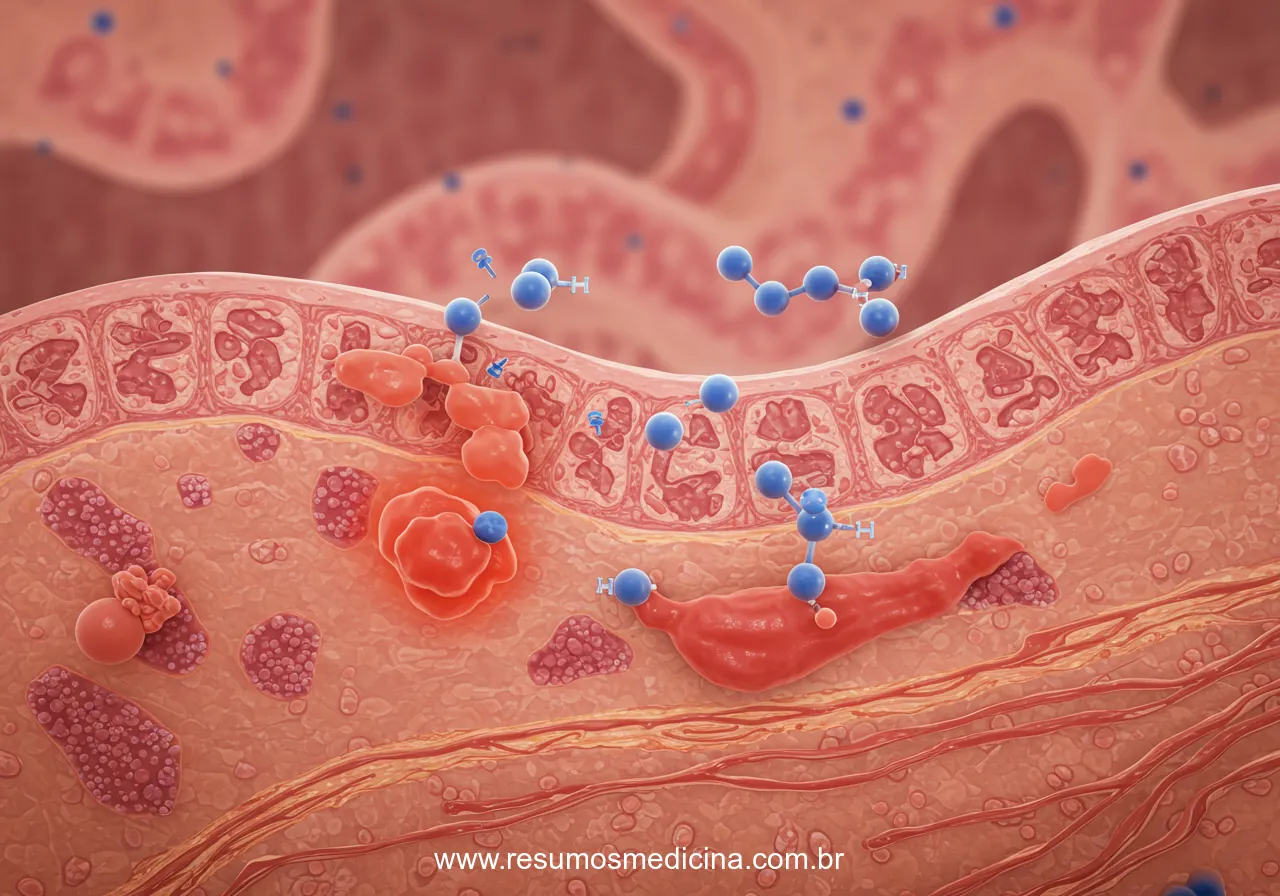
O manejo farmacológico das Doenças Inflamatórias Intestinais (DII), que englobam a Doença de Crohn (DC) e a Retocolite Ulcerativa (RCU), fundamenta-se em objetivos terapêuticos claros e princípios estratégicos essenciais para a prática clínica. O propósito central do tratamento é modificar o curso natural da doença, visando não apenas o controle sintomático, mas também a alteração dos desfechos a longo prazo. Este artigo explora as opções farmacológicas para Doença de Crohn e Retocolite Ulcerativa, incluindo 5-ASA, corticoides, imunomoduladores, agentes biológicos (Anti-TNF, anti-integrinas, anti-IL-12/23) e outras terapias, abordando desde os princípios e objetivos do tratamento até o manejo de situações específicas e considerações importantes sobre segurança e gestação.
Princípios e Objetivos do Tratamento Farmacológico da DII
Os objetivos fundamentais da farmacoterapia nas DII incluem:
- Indução da Remissão: Controlar rapidamente a atividade inflamatória aguda para aliviar os sintomas e iniciar o processo de recuperação da mucosa intestinal.
- Manutenção da Remissão: Sustentar o estado de inatividade da doença a longo prazo, prevenindo recidivas e a progressão do dano intestinal.
- Controle da Inflamação: Reduzir e suprimir a resposta inflamatória subjacente, que é a causa primária das manifestações clínicas e das complicações.
- Alívio dos Sintomas: Melhorar os sintomas debilitantes como diarreia, dor abdominal, sangramento retal e fadiga, restaurando a funcionalidade diária do paciente.
- Prevenção de Complicações: Minimizar o risco de complicações associadas à inflamação crônica, como estenoses, fístulas, abscessos, megacólon tóxico, displasia e necessidade de intervenções cirúrgicas.
- Promoção da Cicatrização da Mucosa: Alcançar a cicatrização endoscópica, um marcador importante de controle inflamatório profundo e associado a melhores prognósticos a longo prazo.
- Melhora da Qualidade de Vida: Restaurar a capacidade funcional e o bem-estar global do paciente, permitindo a retomada de atividades sociais, profissionais e pessoais.
A seleção da estratégia terapêutica é um processo individualizado, crucial para otimizar a eficácia e a segurança do tratamento. Diversos fatores devem ser ponderados na escolha do regime farmacológico:
- Gravidade da Doença: Avaliação da atividade inflamatória, que direciona a intensidade da terapia inicial e de manutenção.
- Localização e Extensão da Doença: O segmento do trato gastrointestinal acometido influencia a escolha da formulação e da classe de fármaco.
- Resposta a Tratamentos Prévios: Histórico de eficácia, intolerância ou refratariedade a terapias anteriores, incluindo a presença de dependência de corticosteroides.
- Características Individuais do Paciente: Idade, comorbidades, estado nutricional, preferências do paciente e considerações especiais como gestação.
- Perfil de Segurança dos Fármacos: Avaliação do risco-benefício de cada opção terapêutica, considerando potenciais efeitos adversos.
- Presença de Manifestações Extraintestinais e Complicações: A coexistência de condições como pioderma gangrenoso ou fístulas perianais na DC exige abordagens terapêuticas específicas.
Com base nestes princípios, o clínico pode definir a abordagem farmacológica mais apropriada, utilizando as diversas classes terapêuticas disponíveis de forma estratégica e sequencial para alcançar os objetivos terapêuticos estabelecidos para cada paciente com DII.
Aminosalicilatos (5-ASA e Derivados): Base do Tratamento da RCU Leve a Moderada
Os aminossalicilatos, que incluem a mesalazina (ácido 5-aminossalicílico ou 5-ASA) e seu precursor, a sulfassalazina, constituem a terapia de primeira linha para a Retocolite Ulcerativa (RCU) de atividade leve a moderada. Sua principal função é controlar a inflamação na mucosa intestinal, sendo eficazes tanto na indução quanto na manutenção da remissão da doença.
Mecanismo de Ação e Eficácia
O mecanismo de ação primordial dos aminossalicilatos ocorre topicamente na mucosa do cólon. O 5-ASA inibe a produção de mediadores inflamatórios cruciais, como prostaglandinas e leucotrienos, por meio da inibição de vias enzimáticas como a ciclooxigenase (COX) e a lipoxigenase (LOX). Adicionalmente, exerce atividade antioxidante, contribuindo para a redução do estresse oxidativo local associado à inflamação intestinal. Esta ação anti-inflamatória localizada é fundamental para aliviar os sintomas e promover a cicatrização da mucosa em pacientes com RCU.
Formas de Administração e Indicações Específicas
A mesalazina (5-ASA) pode ser administrada por via oral ou retal, e a escolha depende da extensão e da gravidade da doença:
- Via Oral: Utilizada para acometimento mais extenso do cólon. Diversas formulações com diferentes mecanismos de liberação garantem a entrega do 5-ASA em segmentos específicos do intestino.
- Via Retal (Supositórios e Enemas): É a via preferencial para o tratamento da proctite ulcerativa e da retossigmoidite, onde a inflamação está confinada às porções mais distais do cólon. Proporciona altas concentrações locais do fármaco com menor absorção sistêmica.
A mesalazina é indicada tanto para a indução da remissão em surtos leves a moderados quanto para a manutenção da remissão a longo prazo, visando prevenir recidivas.
Sulfassalazina: Metabolismo e Efeitos Adversos
A sulfassalazina é uma pró-droga composta por uma molécula de 5-ASA ligada a uma molécula de sulfapiridina através de uma ligação azo. Esta ligação é clivada pelas bactérias presentes no cólon, liberando ambos os componentes. O 5-ASA exerce sua ação anti-inflamatória local, enquanto a sulfapiridina é absorvida sistemicamente e está associada à maioria dos efeitos adversos do fármaco. Estes incluem:
- Efeitos comuns: Náuseas, vômitos, anorexia, cefaleia.
- Efeitos menos comuns e mais graves (hipersensibilidade): Erupções cutâneas, discrasias sanguíneas (como agranulocitose, anemia aplásica).
Devido ao perfil de efeitos adversos associado à sulfapiridina, as formulações de mesalazina são frequentemente preferidas atualmente, embora a sulfassalazina permaneça uma opção terapêutica relevante. É importante notar que a sulfassalazina pode interferir na absorção de folato, sendo recomendada a suplementação em pacientes que a utilizam.
Corticosteroides: Indução Rápida da Remissão e Limitações
Os corticosteroides, incluindo fármacos como prednisona, metilprednisolona, hidrocortisona e budesonida, representam uma classe terapêutica essencial no manejo da Doença Inflamatória Intestinal (DII), particularmente na abordagem da doença ativa. Sua principal contribuição reside na capacidade de indução rápida da remissão, resultado de sua potente ação anti-inflamatória e imunossupressora, que atua suprimindo a resposta imune e reduzindo a inflamação da parede intestinal.
São frequentemente empregados para induzir a remissão em exacerbações de atividade moderada a grave, tanto na Retocolite Ulcerativa (RCU) quanto na Doença de Crohn (DC).
Budesonida: Uma Opção com Menor Efeito Sistêmico
A budesonida se destaca por sua farmacocinética particular. Trata-se de um corticosteroide com elevada atividade anti-inflamatória local, especialmente no íleo terminal e cólon ascendente, mas com baixa biodisponibilidade sistêmica. Isso ocorre devido ao seu extenso metabolismo de primeira passagem no fígado, o que minimiza os efeitos colaterais sistêmicos. Por essa razão, é uma opção terapêutica direcionada para casos de Doença de Crohn ileocecal de atividade leve a moderada. No entanto, sua eficácia para a manutenção da remissão a longo prazo é limitada.
Uso Intravenoso em Casos Graves
Em situações de maior gravidade, como na RCU grave, colite fulminante ou megacólon tóxico, os corticosteroides administrados por via intravenosa (ex: metilprednisolona, hidrocortisona) constituem a terapia de primeira linha. Este manejo geralmente requer ambiente hospitalar para monitorização rigorosa do paciente, especialmente no megacólon tóxico, devido ao risco de mascaramento de sinais de perfuração intestinal e aumento da suscetibilidade a infecções oportunistas.
Limitações Importantes e Efeitos Adversos
Apesar da sua notável eficácia na fase aguda, os corticosteroides não são recomendados para a terapia de manutenção a longo prazo na DII. Esta limitação fundamental advém do seu perfil significativo de efeitos adversos associados ao uso prolongado. Entre os mais relevantes estão: risco aumentado de infecções, osteopenia/osteoporose, diabetes mellitus, hipertensão arterial e ganho de peso. A incapacidade de retirar o corticoide sem reativar a doença define a condição de dependência de corticosteroides, sinalizando a necessidade de otimizar a estratégia terapêutica com agentes poupadores de corticoides (imunomoduladores ou biológicos).
Agentes Biológicos Anti-TNF: Tratamento de Casos Moderados a Graves e Fistulizantes
Os agentes biológicos que atuam como antagonistas do Fator de Necrose Tumoral alfa (Anti-TNF) representam uma classe terapêutica fundamental no manejo da Doença Inflamatória Intestinal (DII), particularmente nos casos de Doença de Crohn (DC) e Retocolite Ulcerativa (RCU) com atividade moderada a grave, ou naqueles refratários às terapias convencionais.
Mecanismo de Ação
O Fator de Necrose Tumoral alfa (TNF-α) é uma citocina pró-inflamatória central na patogênese da DII, desempenhando um papel crucial na perpetuação da inflamação crônica no trato gastrointestinal. Os agentes anti-TNF, como o infliximabe, adalimumabe e golimumabe, são anticorpos monoclonais que atuam neutralizando a atividade do TNF-α. Isso ocorre através da ligação direta à citocina solúvel ou ao TNF-α ligado à membrana celular, bloqueando sua interação com os receptores de superfície celular (TNFR) e, consequentemente, interrompendo a cascata inflamatória subsequente.
Indicações Terapêuticas
Os agentes anti-TNF são indicados para a indução e manutenção da remissão em pacientes com DC e RCU de atividade moderada a grave que apresentaram resposta inadequada, perda de resposta ou intolerância às terapias convencionais, como aminosalicilatos, corticosteroides e/ou imunomoduladores (azatioprina, 6-mercaptopurina). A refratariedade ao tratamento convencional ou a dependência de corticosteroides são, portanto, indicações clássicas para a introdução desta classe terapêutica.
Especificamente na Doença de Crohn, os agentes anti-TNF demonstraram eficácia significativa no tratamento da doença fistulizante, uma complicação comum e debilitante. Esses agentes podem promover o fechamento das fístulas e controlar a inflamação transmural associada. Além disso, em cenários de RCU aguda grave ou colite fulminante refratária à corticoterapia intravenosa, o infliximabe pode ser considerado como terapia de resgate para induzir a remissão.
Administração e Terapia Combinada
Os principais agentes anti-TNF utilizados na DII incluem o infliximabe, o adalimumabe e o golimumabe. O adalimumabe é administrado por via subcutânea. A combinação de um agente anti-TNF com um imunomodulador tiopurínico (azatioprina ou 6-mercaptopurina) é uma estratégia frequentemente empregada. Esta abordagem combinada demonstrou aumentar as taxas de remissão clínica e endoscópica, além de reduzir o risco de desenvolvimento de anticorpos anti-droga, o que pode prolongar a eficácia do agente biológico a longo prazo.
Considerações de Segurança
O uso de agentes anti-TNF requer monitoramento rigoroso devido a potenciais efeitos adversos significativos. As principais considerações de segurança incluem:
- Risco de Infecções: Há um risco aumentado de infecções, incluindo infecções oportunistas. A vigilância para sinais e sintomas de infecção é crucial durante o tratamento.
- Reativação de Tuberculose Latente: O TNF-α é essencial para a manutenção dos granulomas que contêm o Mycobacterium tuberculosis. Sua inibição pode levar à reativação da doença. Portanto, o rastreamento para tuberculose latente é mandatório antes do início da terapia anti-TNF.
- Risco de Linfoma: Observou-se uma associação com um risco ligeiramente aumentado de desenvolvimento de linfomas, em particular o linfoma de células T hepatoesplênico, que é raro mas grave, especialmente em pacientes jovens do sexo masculino em terapia combinada com tiopurinas.
- Outros Efeitos Adversos: Podem ocorrer reações infusionais (no caso de agentes intravenosos), desenvolvimento de anticorpos anti-droga, exacerbação ou desenvolvimento de insuficiência cardíaca congestiva em pacientes predispostos, surgimento de doenças desmielinizantes, reações cutâneas diversas e citopenias.
Outras Classes de Agentes Biológicos: Anti-Integrinas e Anti-IL-12/23
Para além dos agentes bloqueadores do Fator de Necrose Tumoral (anti-TNF), o arsenal terapêutico biológico para a Doença Inflamatória Intestinal (DII) inclui outras classes com mecanismos de ação distintos. Estas terapias representam opções importantes, particularmente para pacientes com Retocolite Ulcerativa (RCU) ou Doença de Crohn (DC) de atividade moderada a grave que não responderam adequadamente ou são intolerantes às terapias convencionais e/ou aos próprios anti-TNF. As principais classes adicionais são os anti-integrinas e os anti-IL-12/23.
Agentes Anti-Integrina
Os agentes anti-integrina atuam sobre a migração leucocitária para o intestino. A molécula alvo principal nesta classe é a integrina α4β7. O vedolizumabe é um anticorpo monoclonal humanizado que se liga especificamente a esta integrina, expressa em linfócitos T circulantes. Ao bloquear a interação da integrina α4β7 com a sua ligante (MAdCAM-1) no endotélio vascular intestinal, o vedolizumabe inibe seletivamente a migração de leucócitos para o tecido gastrointestinal inflamado. Este mecanismo reduz o recrutamento de células imunes para a mucosa intestinal, diminuindo a inflamação local.
O vedolizumabe é indicado para o tratamento da RCU e DC moderada a grave, sendo uma opção terapêutica valiosa em pacientes com resposta inadequada, perda de resposta ou intolerância a corticosteroides, imunomoduladores ou agentes anti-TNF.
Agentes Anti-IL-12/23
Outra classe de agentes biológicos atua sobre as interleucinas (IL) 12 e 23, citocinas chave na patogênese da inflamação crónica na DII. O ustekinumabe é um anticorpo monoclonal humano que se liga à subunidade proteica p40, partilhada pelas citocinas IL-12 e IL-23. A IL-12 está envolvida na diferenciação de células T auxiliares do tipo 1 (Th1), enquanto a IL-23 promove a via Th17. Ao neutralizar ambas as citocinas, o ustekinumabe interfere nestas vias pró-inflamatórias, modulando a resposta imune e reduzindo a inflamação intestinal.
O ustekinumabe é também uma opção terapêutica importante para pacientes com RCU ou DC moderada a grave, especialmente aqueles que falharam ou foram intolerantes a terapias convencionais ou a agentes anti-TNF. A sua inclusão no tratamento permite abordar a doença através de um mecanismo imunomodulador distinto.
A seleção entre estas diferentes classes de biológicos (anti-TNF, anti-integrina, anti-IL-12/23) deve ser individualizada, considerando o histórico terapêutico do paciente, a extensão e gravidade da doença, o perfil de segurança de cada fármaco e as preferências do paciente.
Terapia Combinada: Potencializando a Eficácia e Durabilidade do Tratamento
No manejo da Doença Inflamatória Intestinal (DII), particularmente nos casos que demonstram refratariedade às abordagens terapêuticas convencionais, a estratégia de terapia combinada representa uma opção valiosa. Esta abordagem consiste na utilização simultânea de diferentes classes de medicamentos, com destaque para a associação de um agente imunobiológico, especificamente um anti-TNF (como infliximabe ou adalimumabe), com um imunomodulador da classe das tiopurinas (azatioprina ou 6-mercaptopurina).
A combinação de um agente anti-TNF com uma tiopurina é frequentemente empregada no tratamento da DII refratária, visando alcançar múltiplos objetivos terapêuticos:
- Aumento das Taxas de Remissão: A associação demonstra potencial para elevar as taxas de remissão clínica e endoscópica.
- Redução da Imunogenicidade: A administração concomitante de um imunomodulador demonstrou reduzir o risco de formação de anticorpos contra o agente anti-TNF.
- Prolongamento da Eficácia: Ao mitigar o desenvolvimento de ADAs, a terapia combinada contribui para a manutenção de níveis terapêuticos do agente biológico.
Assim, a terapia combinada, especialmente a associação entre anti-TNF e tiopurinas, consolida-se como uma estratégia importante para potencializar a resposta terapêutica, aumentar a eficácia e prolongar a durabilidade do tratamento em pacientes com DII, sobretudo nos quadros refratários ou de maior gravidade. Cabe ressaltar que esta abordagem intensifica a imunossupressão, exigindo monitoramento clínico e laboratorial rigoroso para avaliação contínua da eficácia e detecção precoce de potenciais eventos adversos, como o risco ligeiramente aumentado de linfoma associado a essa combinação.
Manejo de Situações Específicas: Colite Grave/Fulminante, Megacólon Tóxico e Papel dos Antibióticos
A Doença Inflamatória Intestinal (DII) pode apresentar quadros de agudização graves, como a colite ulcerativa aguda grave, colite fulminante e megacólon tóxico, que demandam manejo específico e, frequentemente, hospitalização.
Abordagem da Colite Ulcerativa Aguda Grave e Colite Fulminante
O tratamento da Retocolite Ulcerativa (RCU) aguda grave geralmente requer internação hospitalar para estabilização hemodinâmica, suspensão da dieta oral (NPO), reidratação venosa e correção de distúrbios eletrolíticos. A terapia de primeira linha consiste na administração de corticosteroides intravenosos.
Para pacientes com colite fulminante ou RCU grave que não respondem adequadamente à corticoterapia intravenosa (casos refratários), são consideradas terapias de resgate. As opções incluem a ciclosporina intravenosa ou agentes biológicos anti-TNF, como o infliximabe. A escolha entre essas opções deve ser individualizada, baseada no perfil de risco-benefício do paciente. Em casos refratários a essas terapias, a colectomia pode ser necessária. É fundamental monitorar o paciente quanto ao desenvolvimento de complicações como megacólon tóxico e perfuração intestinal.
Manejo Clínico do Megacólon Tóxico
O megacólon tóxico é uma complicação grave que exige suporte clínico intensivo imediato. O manejo inicial inclui:
- Reposição volêmica agressiva e correção de distúrbios eletrolíticos.
- Monitorização contínua dos sinais vitais e do diâmetro do cólon.
- Administração de corticosteroides intravenosos.
- Antibioticoterapia empírica de amplo espectro: É crucial para cobrir bactérias gram-negativas e anaeróbias.
É importante ressaltar que medicamentos como antidiarreicos, opioides e anticolinérgicos devem ser evitados em pacientes com colite fulminante e megacólon tóxico.
Para pacientes com megacólon tóxico que não respondem à terapia inicial com corticosteroides intravenosos, a ciclosporina intravenosa pode ser considerada como terapia de resgate. A descompressão colônica, por aspiração retal ou colonoscopia, pode ser considerada em alguns casos.
O Papel dos Antibióticos na DII
O uso de antibióticos na DII é geralmente restrito a situações específicas e não constitui terapia primária para a inflamação intestinal em si, especialmente na RCU. O uso rotineiro de antibióticos não é recomendado no tratamento primário da RCU, a menos que haja evidência de infecção secundária.
Na Doença de Crohn (DC), antibióticos como metronidazol e ciprofloxacino podem ter um papel no manejo de complicações específicas, tais como:
- Doença perianal, incluindo fístulas.
- Complicações infecciosas secundárias.
Entretanto, mesmo na DC, eles não são considerados a terapia inicial de escolha para a proctite ulcerativa ou para a indução/manutenção da remissão na maioria dos casos de DII. O uso prolongado de antibióticos deve ser evitado devido ao risco de desenvolvimento de resistência bacteriana e outros efeitos adversos.
Considerações Importantes: Segurança, Rastreamento e Gestação
A gestão farmacológica da Doença Inflamatória Intestinal (DII) exige atenção meticulosa a aspectos de segurança, particularmente ao utilizar imunossupressores e agentes biológicos. O rastreamento de condições preexistentes e considerações especiais em populações como gestantes são fundamentais para otimizar os resultados e minimizar riscos.
Riscos Associados aos Imunossupressores e Biológicos
O uso de terapias que modulam ou suprimem o sistema imune, embora eficazes no controle da DII, acarreta riscos intrínsecos que demandam monitorização contínua.
- Infecções Oportunistas: Pacientes em tratamento com imunossupressores e agentes biológicos apresentam risco aumentado para infecções oportunistas.
- Reativação de Tuberculose Latente (TBL): A terapia com agentes anti-TNF pode induzir a reativação de TBL.
- Risco de Linfoma: Há uma associação documentada entre o uso de agentes anti-TNF e um risco ligeiramente aumentado de desenvolvimento de linfoma.
- Outros Efeitos Adversos: Além das infecções e do risco de linfoma, a terapia anti-TNF pode cursar com reações infusionais, desenvolvimento de anticorpos anti-droga. Imunomoduladores requerem monitorização para mielossupressão. A ciclosporina está associada a nefrotoxicidade e hipertensão. O uso prolongado de corticosteroides está associado a efeitos sistêmicos significativos, incluindo osteoporose, ganho de peso, hipertensão e diabetes.
Rastreamento de Tuberculose Latente
Devido ao risco de reativação, o rastreamento para TBL é mandatório antes do início de terapia imunossupressora, especialmente com agentes anti-TNF. Este rastreamento deve incluir:
- Teste Tuberculínico (PPD ou Mantoux) e/ou Ensaio de Liberação de Interferon Gama (IGRA).
- Tratamento da TBL: Um resultado positivo necessita de investigação complementar e tratamento adequado.
Manejo da DII na Gestação
O tratamento da DII durante a gestação requer uma avaliação criteriosa do risco-benefício para a mãe e o feto, com o objetivo primário de manter a doença em remissão ou com atividade mínima, controlando a inflamação.
- Avaliação Geral: A decisão terapêutica deve ser individualizada, considerando a gravidade da doença materna e os potenciais riscos fetais de cada fármaco.
- Aminosalicilatos (Mesalazina, Sulfassalazina): São geralmente considerados seguros durante a gestação e amamentação. Contudo, a sulfassalazina pode interferir na absorção de folato, sendo recomendada a suplementação de ácido fólico.
- Antibióticos: O uso, incluindo metronidazol, deve ser cauteloso. A decisão deve ponderar os riscos e benefícios, otimizando a escolha do fármaco, dose e duração.
- Imunomoduladores (Azatioprina, 6-Mercaptopurina): Podem ser considerados em casos de DII mais graves ou refratários durante a gestação.
- Agentes Anti-TNF: Podem ser utilizados em gestantes com DII que não respondem a outras terapias. Há preferência pelo certolizumabe pegol devido à sua menor passagem placentária.
- Metotrexato: É absolutamente contraindicado durante a gestação por ser teratogênico. Mulheres em idade fértil devem utilizar contracepção eficaz durante o tratamento e por um período após a sua suspensão.
Manejo Farmacológico da Refratariedade e Condições Associadas
A gestão da Doença Inflamatória Intestinal (DII), particularmente da Retocolite Ulcerativa (RCU), frequentemente encontra desafios relacionados à ausência de resposta terapêutica adequada ou à dependência de certas classes de medicamentos. A compreensão e o manejo dessas situações, bem como das condições associadas à DII, são cruciais para otimizar os desfechos clínicos.
Abordagem da Refratariedade e Dependência de Corticosteroides na RCU
A intratabilidade clínica na RCU é definida pela falha do tratamento médico convencional em controlar adequadamente a atividade inflamatória e os sintomas. Especificamente, a refratariedade ao tratamento convencional é caracterizada pela falta de resposta a aminosalicilatos e/ou imunomoduladores. Já a dependência de corticosteroides se manifesta pela necessidade contínua desses agentes para manter a remissão ou pela incapacidade de reduzir suas doses sem provocar exacerbação da doença. Ambas as condições são indicativas da necessidade de intensificação terapêutica.
As estratégias para manejo incluem:
- Terapia Biológica: Constitui uma opção terapêutica fundamental. As classes principais incluem:
- Anti-TNF: Agentes como infliximabe, adalimumabe e golimumabe.
- Anti-integrina: O vedolizumabe.
- Anti-IL-12/23: O ustekinumabe.
A seleção do agente biológico é individualizada, considerando histórico, segurança e custos.
- Imunomoduladores em Combinação: A terapia combinada pode aumentar as taxas de remissão.
- Ciclosporina: Imunossupressor que pode ser considerado como terapia de resgate.
- Colectomia: Permanece uma opção terapêutica importante diante da intratabilidade clínica.
Manejo Farmacológico de Condições Associadas
Além do controle da inflamação intestinal, o manejo da DII envolve a abordagem de manifestações extraintestinais e complicações, como o pioderma gangrenoso e a doença óssea metabólica.
- Pioderma Gangrenoso: O tratamento desta manifestação cutânea visa controlar a inflamação e promover a cicatrização. A abordagem farmacológica inclui:
- Corticosteroides Sistêmicos.
- Imunossupressores: Ciclosporina, azatioprina e infliximabe.
É fundamental otimizar o tratamento da DII subjacente para o manejo eficaz do pioderma gangrenoso.
- Osteopenia e Osteoporose: São complicações comuns na DII. A prevenção e o manejo envolvem:
- Otimização do tratamento da DII.
- Suplementação adequada de cálcio e vitamina D.
- Estímulo à prática regular de exercícios físicos.
Consideração de terapias específicas para osteoporose em casos selecionados.
Conclusão
O tratamento farmacológico da DII é complexo e multifacetado, exigindo uma abordagem individualizada que considere a gravidade e extensão da doença, a resposta a tratamentos prévios, as características do paciente e o perfil de segurança dos fármacos. Desde os aminossalicilatos, como base para casos leves a moderados de RCU, até os agentes biológicos, como anti-TNF, anti-integrinas e anti-IL-12/23, para casos mais graves ou refratários, as opções terapêuticas são vastas e em constante evolução. A terapia combinada, o manejo de situações específicas como colite fulminante e megacólon tóxico, e a atenção às considerações de segurança, rastreamento e gestação são componentes cruciais para otimizar os resultados e melhorar a qualidade de vida dos pacientes com DII. A refratariedade terapêutica e as condições associadas exigem estratégias específicas e intensificação do tratamento, visando sempre o controle da inflamação e a prevenção de complicações.