O manejo adequado do melanoma cutâneo exige uma abordagem diagnóstica e terapêutica precisa, iniciando-se com a correta identificação e avaliação da lesão primária. A cirurgia é a principal modalidade de tratamento para o melanoma localizado, e a avaliação do estado linfonodal regional é fundamental para o estadiamento preciso e a definição de estratégias terapêuticas subsequentes.
Diagnóstico Inicial: A Importância da Biópsia Excisional
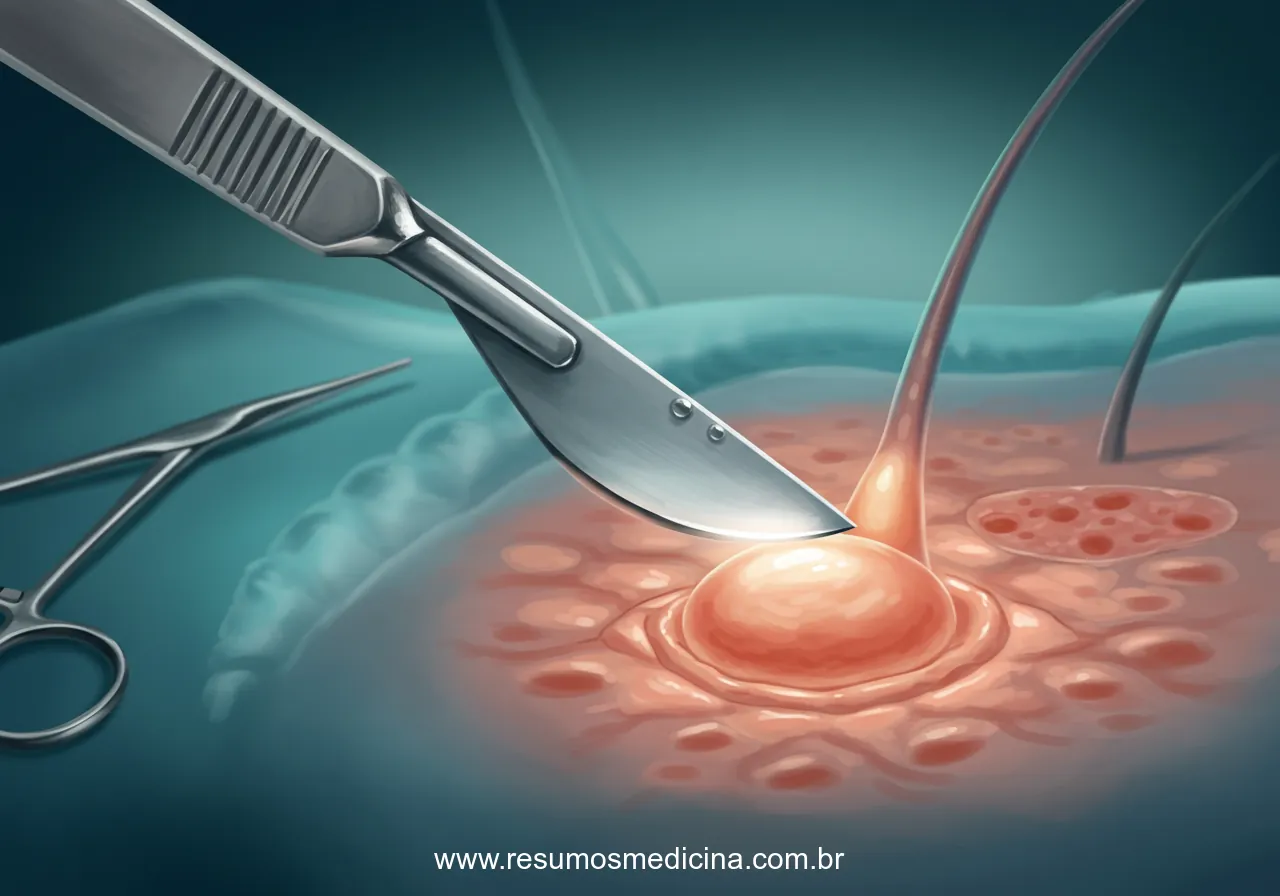
A abordagem padrão-ouro para o diagnóstico de lesões cutâneas com suspeita clínica de melanoma é a biópsia excisional. Este procedimento visa a remoção completa da lesão clinicamente visível, incluindo uma margem radial estreita de pele macroscopicamente normal, tipicamente variando entre 1 a 3 milímetros. A escolha por margens estreitas nesta fase inicial é uma decisão técnica fundamental com múltiplos propósitos.
Primeiramente, assegura a integridade da amostra e a preservação da arquitetura tecidual, permitindo uma análise histopatológica completa e fidedigna. Isso é indispensável para a determinação de fatores prognósticos cruciais, como a espessura de Breslow (profundidade máxima de invasão tumoral), a presença ou ausência de ulceração, o índice mitótico, o nível de Clark, e outros marcadores histológicos que impactam diretamente o estadiamento TNM e orientam as decisões terapêuticas subsequentes.
Secundariamente, a utilização de margens estreitas evita a distorção anatômica e a interrupção dos vasos linfáticos da derme, preservando o padrão de drenagem linfática regional original. Este cuidado é essencial, pois a aplicação de margens amplas na biópsia inicial pode comprometer ou até inviabilizar a posterior identificação precisa do linfonodo sentinela, caso a pesquisa deste (Pesquisa de Linfonodo Sentinela – PLS, ou Sentinel Lymph Node Biopsy – SLNB) seja indicada após a confirmação histopatológica de melanoma invasivo. A remoção excessiva de tecido pode alterar as vias de drenagem, dificultando a localização do linfonodo que primariamente receberia as células metastáticas.
Embora a biópsia incisional (remoção de apenas um fragmento da lesão) possa ser considerada em cenários específicos, como lesões muito extensas (onde a excisão completa resultaria em morbidade significativa) ou em localizações anatomicamente complexas (face, dígitos), ela deve ser evitada sempre que possível. A principal limitação da biópsia incisional é o risco significativo de subestimar a verdadeira profundidade de invasão (Breslow) e outras características histopatológicas críticas do tumor, o que pode levar a um estadiamento incorreto e a um planejamento terapêutico inadequado.
Independentemente da técnica utilizada, a amostra obtida deve ser manuseada cuidadosamente, adequadamente fixada (geralmente em formalina tamponada a 10%) e enviada para análise por um patologista com experiência comprovada em dermatopatologia, garantindo a acurácia do diagnóstico e da avaliação prognóstica.
Princípios Técnicos da Biópsia Excisional Diagnóstica
- Remoção Completa: Excisar a totalidade da lesão suspeita.
- Margens Estreitas (1-3 mm): Incluir uma pequena margem radial de pele normal para garantir a remoção completa sem comprometer a futura pesquisa de linfonodo sentinela ou a excisão definitiva com margens ampliadas.
- Profundidade Adequada: A excisão deve incluir a derme reticular profunda ou até o tecido subcutâneo para assegurar a avaliação completa da espessura tumoral.
- Orientação da Incisão: Sempre que possível, especialmente nos membros e tronco, a incisão elíptica deve ser orientada longitudinalmente, seguindo a direção da drenagem linfática regional e as linhas de tensão da pele (linhas de Langer), para otimizar o resultado estético e minimizar a interferência com o mapeamento linfático futuro.
- Manuseio e Fixação: Cuidados na manipulação da peça cirúrgica para evitar artefatos e fixação apropriada para preservar as características histológicas.
Tratamento Cirúrgico Primário: Excisão Ampla com Margens Adequadas
Após a confirmação histopatológica do diagnóstico de melanoma e a determinação de seus fatores prognósticos, notadamente a espessura de Breslow, o tratamento primário para a doença localizada consiste na excisão cirúrgica ampla. Este procedimento, também conhecido como Excisão Local Ampliada (ELA) ou ampliação de margens, sucede a biópsia excisional inicial e visa erradicar quaisquer células neoplásicas residuais. A obtenção de margens cirúrgicas microscopicamente livres de tumor é um pilar essencial para o controle oncológico local.
A definição da extensão das margens cirúrgicas é fundamentalmente guiada pela espessura de Breslow do melanoma primário. O objetivo é assegurar a remoção completa do tumor, incluindo possíveis extensões subclínicas ou micrometástases locais, minimizando assim o risco de recorrência local da doença. Margens de ressecção insuficientes estão associadas a um prognóstico desfavorável devido ao maior risco de recidiva.
Recomendações de Margens Cirúrgicas Laterais Baseadas na Espessura de Breslow
As diretrizes clínicas, baseadas em extensos estudos, estabelecem recomendações para as margens laterais de tecido normal a serem excisadas ao redor da cicatriz da biópsia ou da lesão primária, estratificadas pela espessura de Breslow:
- Melanoma in situ (Tis): Margem de 0,5 cm a 1,0 cm.
- Melanoma invasivo com espessura ≤ 1,0 mm: Margem de 1,0 cm.
- Melanoma invasivo com espessura > 1,0 mm e ≤ 2,0 mm (1,01 mm a 2,0 mm): Margem de 1,0 cm a 2,0 cm. A escolha dentro deste intervalo pode ser individualizada; alguns protocolos sugerem considerar 2,0 cm, enquanto outros admitem 1,0 cm dependendo de características específicas do tumor e do paciente.
- Melanoma invasivo com espessura > 2,0 mm: Margem de 2,0 cm.
É importante notar que, embora estas sejam as recomendações gerais, a decisão final sobre as margens pode exigir individualização. Em localizações anatômicas complexas, como a face ou extremidades distais, onde a preservação da função e da estética são considerações importantes, margens mais estreitas podem ser aceitas, desde que a segurança oncológica não seja comprometida. Tais decisões devem ser criteriosamente avaliadas, preferencialmente em contexto multidisciplinar.
Adicionalmente, durante o planejamento da ELA, a orientação da incisão elíptica pode ser feita seguindo as linhas de tensão da pele (linhas de Langer), quando tecnicamente viável. Essa prática visa otimizar o resultado cosmético e funcional da cicatrização, minimizando a tensão na ferida operatória. No entanto, a prioridade inegociável permanece a garantia de margens oncológicas adequadas para o controle efetivo da doença.
Avaliação Linfonodal: O Conceito, Técnica e Importância do Linfonodo Sentinela (LS)
A avaliação do estado dos linfonodos regionais é um passo crucial no estadiamento e na definição da estratégia terapêutica para o melanoma cutâneo, uma vez que a disseminação linfática é uma via primária de metástase para este tipo de neoplasia. Central a esta avaliação está o conceito de Linfonodo Sentinela (LS), que se refere ao primeiro linfonodo, ou grupo de linfonodos, que recebe a drenagem linfática diretamente da área onde o tumor primário está localizado. A premissa oncológica é que as células neoplásicas, ao se disseminarem pela via linfática, tenderão a alcançar e se estabelecer primeiramente neste(s) linfonodo(s) específico(s).
A Biópsia do Linfonodo Sentinela (BLS), também conhecida como Pesquisa de Linfonodo Sentinela (PLS ou SLNB), é, portanto, um procedimento cirúrgico de estadiamento fundamental. Sua principal finalidade é detectar a presença de metástases ocultas (micrometástases), que frequentemente não são identificáveis através do exame físico (palpação dos linfonodos) ou por exames de imagem convencionais. Para identificar o LS, utiliza-se uma técnica de mapeamento linfático que geralmente envolve a injeção peritumoral de um radiofármaco (tecnécio-99m) detectado por gama probe (linfocintilografia) e/ou um corante vital azul. O(s) linfonodo(s) que captam estes marcadores são identificados, excisados e submetidos a análise histopatológica detalhada.
Indicações e Contraindicações para a BLS
A indicação da BLS baseia-se no risco estimado de metástase linfonodal oculta. Geralmente, o procedimento é recomendado para melanomas invasivos com:
- Espessura de Breslow > 1,0 mm.
- Espessura de Breslow entre 0,8 mm e 1,0 mm (algumas diretrizes consideram ≥ 0,8 mm) associada a fatores de risco adicionais, como: ulceração, alto índice mitótico, invasão linfovascular ou regressão tumoral significativa.
A BLS não é indicada para:
- Melanoma in situ (Tis), devido ao risco negligenciável de metástase linfática.
- Pacientes com evidência clínica (linfonodos palpáveis e suspeitos) ou radiológica de metástase linfonodal. Nestes casos, a abordagem indicada é a biópsia (por agulha fina ou excisional) do linfonodo suspeito para confirmação histopatológica.
Implicações Prognósticas e Terapêuticas do Status do LS
O status do linfonodo sentinela (positivo ou negativo para metástase) é um dos fatores prognósticos independentes mais importantes no melanoma, influenciando diretamente o estadiamento TNM (componente ‘N’) e as taxas de sobrevida livre de doença (SLD) e sobrevida global (SG).
- LS Negativo: A ausência de metástases no(s) LS sugere baixa probabilidade de envolvimento dos demais linfonodos da cadeia regional e um menor risco de disseminação sistêmica, conferindo um prognóstico mais favorável. Nestes casos, geralmente se evita a linfadenectomia completa (esvaziamento ganglionar), poupando o paciente da morbidade associada a este procedimento mais extenso (ex: linfedema, seroma, lesão nervosa, infecção).
- LS Positivo: A detecção de metástase no LS confirma doença regional (Estágio III), indica risco significativamente aumentado de metástases em outros linfonodos da mesma bacia e de disseminação sistêmica, implicando um prognóstico menos favorável. Este achado geralmente indica a necessidade de linfadenectomia completa da cadeia linfonodal acometida e serve como forte argumento para a indicação de terapia adjuvante sistêmica (como imunoterapia com inibidores de checkpoint ou terapia-alvo para mutações BRAF, quando aplicável) para reduzir o risco de recidiva.
Assim, a pesquisa e biópsia do linfonodo sentinela representam uma ferramenta essencial no manejo contemporâneo do melanoma, fornecendo informações prognósticas críticas e orientando decisões terapêuticas subsequentes, incluindo a extensão da cirurgia linfonodal e a necessidade de tratamentos sistêmicos adjuvantes.
Indicações para a Biópsia do Linfonodo Sentinela (BLS)
A indicação para a realização da biópsia do linfonodo sentinela (BLS), também conhecida como pesquisa de linfonodo sentinela (PLS), é um processo seletivo no manejo do melanoma cutâneo. Este procedimento destina-se a pacientes sem evidência clínica ou radiológica de acometimento linfonodal regional (linfonodos não palpáveis ou suspeitos), mas que apresentam características tumorais associadas a um risco significativo de micrometástases ocultas.
Critérios Baseados na Espessura de Breslow e Fatores de Risco Associados
O principal fator determinante para a recomendação da BLS é a espessura de Breslow, que quantifica a profundidade da invasão tumoral. As indicações geralmente seguem os seguintes critérios, baseados em múltiplas diretrizes e evidências:
- Melanomas com Espessura de Breslow > 1 mm: A BLS é consistentemente recomendada como procedimento padrão para estadiamento neste grupo de pacientes, devido ao risco substancialmente elevado de metástase linfonodal oculta.
- Melanomas com Espessura de Breslow entre 0,8 mm e 1,0 mm: Para melanomas invasivos nesta faixa de espessura (limiar inferior por vezes citado como 0,75 mm ou 0,76 mm em algumas fontes), a indicação da BLS é condicional e fortemente considerada na presença de um ou mais dos seguintes fatores de risco adicionais, que aumentam a probabilidade de envolvimento linfonodal:
- Ulceração: A presença de ulceração histológica no tumor primário é um fator prognóstico adverso independente e um forte indicador para a BLS, sendo frequentemente recomendada mesmo em melanomas com espessura ≤ 1 mm.
- Alto Índice Mitótico: Uma taxa mitótica elevada (número de mitoses por mm²) reflete maior atividade proliferativa e associa-se a um risco aumentado de disseminação metastática.
- Invasão Linfovascular: A detecção histopatológica de células neoplásicas no interior de vasos linfáticos ou sanguíneos peritumorais.
- Regressão Tumoral Significativa: Embora seu significado prognóstico seja debatido, a presença de áreas extensas de regressão pode indicar um comportamento biológico potencialmente mais agressivo ou dificultar a avaliação precisa da espessura máxima, sendo considerado um fator em algumas diretrizes.
- Microssatélites: Identificação de ninhos tumorais microscópicos distintos, porém próximos (<2 cm) ao tumor primário.
É importante salientar que a indicação da BLS fundamenta-se nessas características do tumor primário (espessura e fatores de risco), e não primariamente no subtipo histológico do melanoma. A decisão final sobre a realização da BLS deve ser individualizada, considerando o perfil completo de risco do tumor, as condições clínicas do paciente e alinhada às diretrizes clínicas institucionais e internacionais vigentes, que podem apresentar pequenas variações nos limiares exatos.
Situações em que a BLS Não é Indicada (Contraindicações)
Existem cenários clínicos específicos nos quais a BLS não é recomendada ou perde sua utilidade:
- Evidência Clínica ou Radiológica de Metástase Linfonodal: Em pacientes com linfonodos regionalmente aumentados, endurecidos, fixos ou suspeitos à palpação, ou com metástases linfonodais confirmadas por exames de imagem ou biópsia prévia (ex: Punção Aspirativa por Agulha Fina – PAAF ou biópsia excisional de linfonodo), a BLS é desnecessária. O estadiamento nodal já é considerado positivo, e a abordagem direciona-se à confirmação histopatológica e ao tratamento da doença macroscopicamente evidente, geralmente através de linfadenectomia completa.
- Melanoma in situ (Tis): Lesões confinadas à epiderme, como o lentigo maligno não invasivo, apresentam um risco considerado negligível ou mínimo de metástase linfática. Portanto, a BLS não está indicada para esta forma da doença.
- Melanomas Finos Sem Fatores de Risco Adicionais: Melanomas invasivos com espessura de Breslow ≤ 0,8 mm (ou ≤ 0,76 mm) que não apresentam ulceração ou quaisquer outros fatores de alto risco mencionados anteriormente possuem uma probabilidade muito baixa de metástase linfonodal. Nestes casos, a BLS geralmente não é realizada devido ao baixo rendimento diagnóstico e ao risco mínimo de falso negativo clinicamente relevante.
Procedimento da Biópsia do Linfonodo Sentinela: Mapeamento e Técnica
A execução da Biópsia do Linfonodo Sentinela (BLS) envolve uma abordagem técnica padronizada que se inicia com o mapeamento pré-operatório e culmina na excisão e análise histopatológica do(s) linfonodo(s) identificado(s).
Mapeamento Linfático Pré-operatório: Linfocintilografia
O mapeamento pré-operatório é convencionalmente realizado através da linfocintilografia. Este exame de imagem funcional consiste na injeção intradérmica de um radiofármaco, tipicamente um radiocolóide (como o tecnécio-99m), nas proximidades do sítio do melanoma primário ou da cicatriz da biópsia excisional. O radiofármaco é transportado pelo sistema linfático e se concentra preferencialmente no(s) primeiro(s) linfonodo(s) que drenam a região – o(s) linfonodo(s) sentinela(s). A detecção e localização desses linfonodos são realizadas por meio de uma gama câmera. É importante notar que linfonodos com hipercaptação identificados na linfocintilografia representam os prováveis linfonodos sentinelas, mas a captação aumentada pode também ser decorrente de condições inflamatórias não neoplásicas.
Identificação Intraoperatória e Técnica Cirúrgica
Durante o procedimento cirúrgico, a localização precisa do(s) linfonodo(s) sentinela(s) mapeado(s) é confirmada utilizando-se uma sonda gama portátil (gamma probe), que detecta a radioatividade emitida pelo radiofármaco acumulado no linfonodo. Frequentemente, para aumentar a acurácia da identificação, essa técnica é combinada com a injeção intradérmica perilesional de um corante azul vital (como o azul patente) minutos antes da incisão cirúrgica. O corante segue o mesmo trajeto linfático do radiofármaco, corando o(s) linfonodo(s) sentinela(s) de azul e permitindo sua visualização direta. A utilização combinada do radiofármaco e do corante azul é frequentemente empregada para maximizar as taxas de detecção do linfonodo sentinela.
Após a identificação intraoperatória por radioatividade e/ou coloração azul, realiza-se a excisão cirúrgica do(s) linfonodo(s) sentinela(s) através de uma incisão cutânea planejada sobre a área identificada. O material excisado é encaminhado para exame histopatológico detalhado, que inclui cortes seriados e, frequentemente, a realização de análise por imuno-histoquímica (utilizando marcadores como Melan-A, HMB-45, SOX10, entre outros) para detectar micrometástases ou células tumorais isoladas com maior sensibilidade.
Manejo Após Avaliação Linfonodal: Condutas Baseadas no Status Nodal
O resultado da avaliação linfonodal regional, seja pela biópsia do linfonodo sentinela (BLS) ou pela investigação de linfonodos clinicamente suspeitos, direciona as etapas subsequentes do tratamento do melanoma.
Conduta Diante de Linfonodo Sentinela Positivo (BLS+)
A identificação de metástase no(s) linfonodo(s) sentinela(s) confirma a presença de doença regional (Estágio III). Em decorrência deste achado, a conduta padrão recomendada é a realização de um esvaziamento ganglionar completo (linfadenectomia) da cadeia linfonodal regional correspondente. O objetivo principal da linfadenectomia neste contexto é obter o controle locorregional da doença, removendo outros possíveis linfonodos acometidos na mesma bacia de drenagem para melhorar o prognóstico. Este estadiamento patológico mais preciso, confirmando o Estágio III, também é fundamental para a decisão sobre terapias sistêmicas adjuvantes, como imunoterapia (inibidores de checkpoint imunológico) ou terapia-alvo (inibidores de BRAF e MEK em pacientes com mutações BRAF), visando reduzir o risco de recidiva sistêmica.
Abordagem de Linfonodos Clinicamente Palpáveis e Suspeitos
Quando o exame físico identifica linfonodos regionalmente aumentados, endurecidos ou fixos, a suspeita de metástase clinicamente evidente é alta. Nestas situações, a investigação diagnóstica prioritária foca na confirmação histopatológica do envolvimento metastático. A Punção Aspirativa por Agulha Fina (PAAF) ou a biópsia excisional do linfonodo são os métodos de escolha para obtenção de amostra tecidual para análise. Uma vez histologicamente confirmada a metástase no linfonodo avaliado, a indicação terapêutica é, similarmente ao cenário pós-BLS positiva, a linfadenectomia regional completa da cadeia ganglionar acometida.
Considerações sobre a Linfadenectomia Regional Completa
O esvaziamento ganglionar, procedimento essencial para o controle oncológico em casos de metástase linfonodal confirmada, é uma cirurgia de maior porte e está associado a potenciais complicações que devem ser discutidas com o paciente. Os riscos inerentes ao procedimento incluem:
- Linfedema: Edema crônico do membro ou região correspondente devido à alteração da drenagem linfática pós-cirúrgica.
- Seroma: Acúmulo de fluido seroso na loja cirúrgica.
- Lesão de Estruturas Nervosas: Pode resultar em déficits motores, dor crônica ou alterações sensitivas.
- Alterações de Sensibilidade: Parestesias (formigamento) ou hipoestesia (diminuição da sensibilidade) na pele da área operada ou adjacências.
- Infecção de Sítio Cirúrgico.
A decisão pela linfadenectomia deve sempre ponderar os benefícios esperados em termos de controle da doença e impacto na sobrevida contra os riscos de morbidade funcional e complicações associadas ao procedimento cirúrgico.
Considerações Adicionais: Lentigo Maligno e Metástases em Trânsito
Para além das abordagens gerais de tratamento cirúrgico e avaliação linfonodal no melanoma, é relevante considerar apresentações específicas como o lentigo maligno e o conceito de metástases em trânsito, que possuem características e implicações próprias no manejo da doença.
Lentigo Maligno e Lentigo Maligno Melanoma
O Lentigo Maligno (LM) representa uma forma de melanoma in situ, caracterizado pela proliferação de melanócitos atípicos confinados à epiderme. Clinicamente, manifesta-se frequentemente em áreas de exposição solar crônica, notadamente na face. A excisão cirúrgica constitui o tratamento padrão. No entanto, a delimitação das margens cirúrgicas para o LM pode ser particularmente desafiadora devido à frequente ausência de limites clínicos nítidos e à possibilidade de extensão subclínica além da lesão visível. As margens recomendadas para a excisão do LM seguem as diretrizes para melanoma in situ, geralmente variando de 0,5 a 1,0 cm, visando a remoção completa da lesão.
Quando o LM progride e demonstra invasão da derme, a lesão é classificada como Lentigo Maligno Melanoma (LMM), representando uma forma invasiva da doença. Neste cenário, a determinação das margens cirúrgicas para a excisão deixa de seguir as recomendações específicas para lesões in situ e passa a ser regida pelas diretrizes padrão aplicáveis aos melanomas invasivos. A largura das margens é, então, definida com base fundamentalmente na espessura de Breslow do componente invasor do tumor, conforme os critérios previamente estabelecidos para melanomas invasivos.
Metástases em Trânsito
Metástases em trânsito são definidas como focos tumorais secundários que surgem na pele ou no tecido subcutâneo, localizados a uma distância superior a 2 cm do sítio do tumor primário (ou da cicatriz de excisão inicial), porém permanecem confinados dentro da bacia de drenagem linfática regional correspondente à lesão primária. A identificação de metástases em trânsito caracteriza uma forma de disseminação loco-regional da doença. Este achado possui implicações prognósticas e terapêuticas, impactando diretamente o estadiamento do melanoma, especificamente influenciando a classificação do componente nodal (‘N’) dentro do sistema TNM.