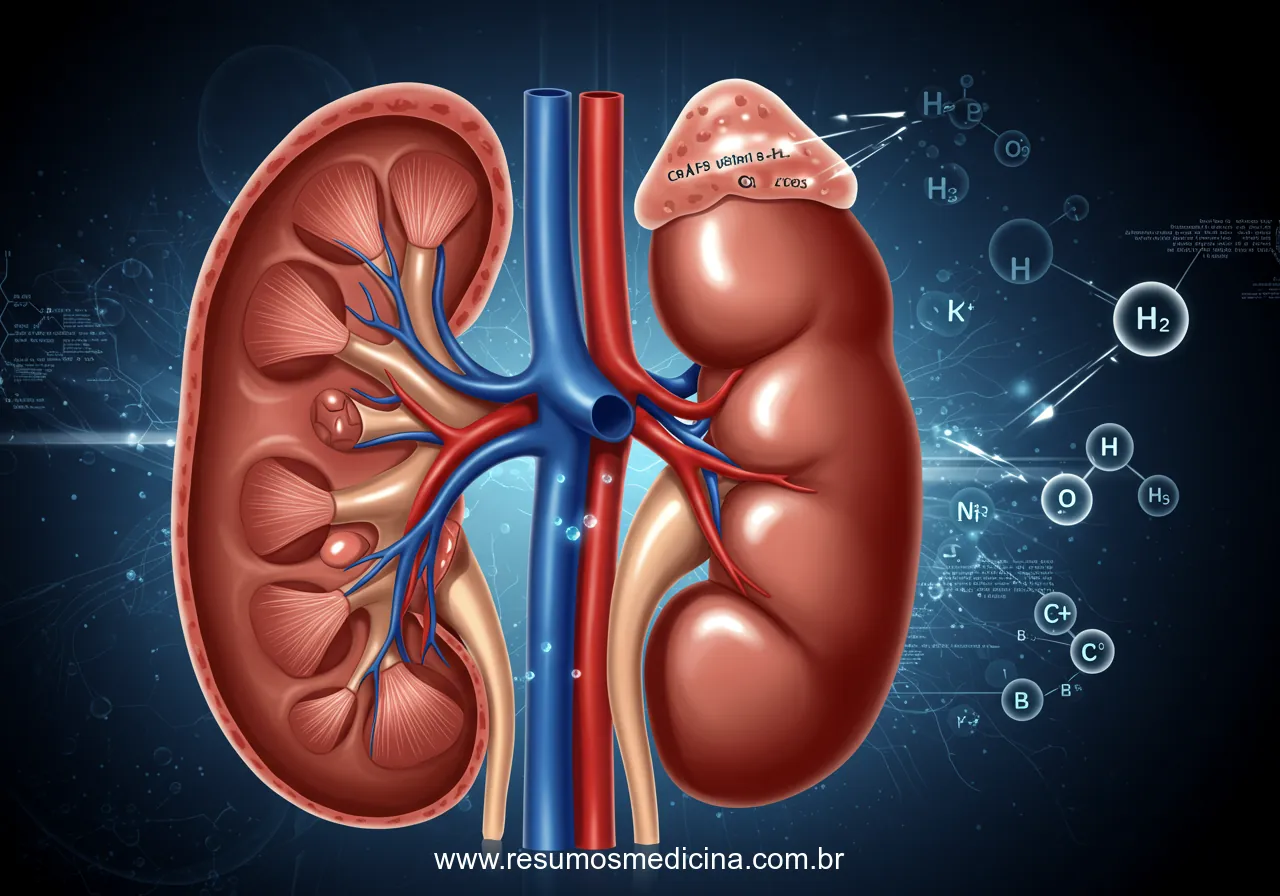
O equilíbrio hidroeletrolítico é crucial para a manutenção da homeostase do organismo, e sua regulação é finamente controlada por hormônios como o ADH (Vasopressina) e o SRAA (Sistema Renina-Angiotensina-Aldosterona). Este artigo explora o papel fundamental desses sistemas hormonais, bem como a importância da aldosterona e da densidade urinária, na regulação do balanço de água e eletrólitos, como sódio e potássio, especialmente em situações de estresse cirúrgico e trauma.
O Hormônio Antidiurético (ADH/Vasopressina) e a Regulação da Água Corporal
O Hormônio Antidiurético (ADH), também conhecido como Vasopressina, desempenha um papel crucial na regulação do balanço hídrico corporal. Este hormônio é secretado pela neurohipófise (hipófise posterior) em resposta a alterações fisiológicas específicas que indicam a necessidade de conservação de água pelo organismo.
Os principais estímulos para a liberação de ADH incluem o aumento da osmolaridade plasmática e a diminuição do volume sanguíneo circulante efetivo. Adicionalmente, a ativação do sistema nervoso simpático, como pode ocorrer em situações de estresse ou trauma, também pode desencadear a secreção de vasopressina. Esses mecanismos garantem que o corpo responda adequadamente a estados de desidratação ou hipovolemia.
A ação primária do ADH ocorre nos rins, especificamente nos túbulos coletores. O hormônio liga-se a receptores nas células principais dessas estruturas, desencadeando uma cascata de sinalização intracelular que culmina na inserção de canais de água, conhecidos como aquaporinas (AQP2), na membrana apical (luminal) das células tubulares. Esse processo aumenta significativamente a permeabilidade da membrana à água.
Com o aumento da permeabilidade, a água é reabsorvida passivamente do filtrado tubular para o interstício medular hipertônico e, subsequentemente, para o sangue, seguindo o gradiente osmótico. Essa reabsorção de água resulta em uma diminuição do volume urinário e um aumento da concentração da urina, fenômeno que contribui para o aumento da densidade urinária. O efeito final é a conservação da água corporal, a manutenção do volume sanguíneo e a estabilização da osmolaridade plasmática, elementos essenciais para a homeostase hídrica. Em concentrações elevadas, a vasopressina também pode induzir vasoconstrição, auxiliando na manutenção da pressão arterial.
Sistema Renina-Angiotensina-Aldosterona (SRAA): Ativação e Funções
O Sistema Renina-Angiotensina-Aldosterona (SRAA) representa um mecanismo hormonal de importância crítica na regulação da pressão arterial e do volume sanguíneo. Sua ativação é desencadeada primariamente por condições que levam à diminuição da pressão arterial ou do volume sanguíneo circulante.
Situações como estresse cirúrgico, frequentemente associado à perda de fluidos, ou trauma, são contextos clínicos comuns onde se observa a ativação do SRAA. Em resposta a esses estímulos hipovolêmicos ou hipotensivos, os rins liberam a enzima renina.
A renina inicia uma cascata bioquímica ao converter o angiotensinogênio plasmático em angiotensina I. Subsequentemente, a angiotensina I é convertida no peptídeo ativo, a angiotensina II, pela ação da Enzima Conversora de Angiotensina (ECA).
A angiotensina II é o principal componente efetor do sistema, exercendo múltiplas funções fisiológicas direcionadas à restauração da homeostase hemodinâmica. Seus efeitos incluem:
- Indução de potente vasoconstrição arteriolar, o que eleva a resistência vascular periférica e a pressão arterial.
- Estímulo direto da secreção de aldosterona pelo córtex das glândulas adrenais.
- Estímulo da sensação de sede, promovendo a ingestão de água.
A aldosterona liberada atua nos túbulos distais e ductos coletores renais, promovendo a reabsorção de sódio e, consequentemente, de água, ao mesmo tempo que aumenta a excreção de potássio e hidrogênio. A retenção de sódio e água resultante eleva o volume sanguíneo. Portanto, através da vasoconstrição e da expansão volêmica mediada pela aldosterona e pela sede, o SRAA atua de forma coordenada para elevar a pressão arterial e restaurar o volume circulante eficaz.
Aldosterona: O Hormônio Mineralocorticoide e o Controle de Sódio e Potássio
A aldosterona é um hormônio esteroide da classe dos mineralocorticoides, produzido e secretado pela zona glomerulosa do córtex da glândula adrenal. Sua regulação e ação são fundamentais para a manutenção do equilíbrio hidroeletrolítico e da pressão arterial, sendo um componente essencial da homeostase corporal.
Estímulos para a Secreção de Aldosterona
A liberação de aldosterona é modulada por múltiplos fatores, sendo os principais:
- Ativação do Sistema Renina-Angiotensina-Aldosterona (SRAA): Este sistema é ativado em resposta a gatilhos como a diminuição do volume sanguíneo ou da pressão arterial, condições frequentemente observadas em contextos de estresse, cirurgia ou trauma. A renina, liberada pelos rins, inicia uma cascata enzimática que resulta na formação de angiotensina II. A angiotensina II atua diretamente sobre as células do córtex adrenal, promovendo a síntese e secreção de aldosterona.
- Aumento da Concentração Plasmática de Potássio (Hipercalemia): Níveis elevados de potássio no plasma constituem um potente estímulo direto para a liberação de aldosterona pelo córtex adrenal, independente do SRAA.
- Diminuição da Concentração Plasmática de Sódio (Hiponatremia): Uma redução nos níveis de sódio plasmático também pode estimular a secreção de aldosterona, embora geralmente em menor grau que a hipercalemia ou a ativação do SRAA.
Ações Renais da Aldosterona
A aldosterona exerce seus efeitos primários nos segmentos finais do néfron, especificamente nos túbulos contorcidos distais e nos túbulos coletores renais. Sua ligação a receptores mineralocorticoides intracelulares desencadeia respostas que alteram o transporte iônico:
- Aumento da Reabsorção de Sódio (Na+): A principal função da aldosterona é intensificar a reabsorção de sódio do filtrado glomerular de volta para a circulação sanguínea. Isso ocorre através do aumento da expressão e atividade de canais de sódio epiteliais (ENaC) na membrana apical e da bomba de Na+/K+-ATPase na membrana basolateral das células principais. A reabsorção de sódio cria um gradiente osmótico que favorece a retenção de água, contribuindo para a manutenção ou restauração do volume extracelular e da pressão arterial.
- Aumento da Excreção de Potássio (K+): Concomitantemente à reabsorção de sódio, a aldosterona promove a secreção ativa de potássio do sangue para o lúmen tubular, facilitando sua eliminação pela urina. Este efeito é crucial para prevenir a hipercalemia.
- Aumento da Excreção de Íons Hidrogênio (H+): A aldosterona também estimula a secreção de prótons (H+) pelas células intercaladas dos túbulos coletores. Esta ação contribui para a excreção de ácido e a manutenção do equilíbrio ácido-básico do organismo, auxiliando na regulação do pH sanguíneo.
Portanto, a aldosterona é um regulador vital da homeostase eletrolítica, particularmente do sódio e do potássio, com implicações diretas no controle do volume do fluido extracelular, na pressão arterial e no equilíbrio ácido-básico.
Implicações Clínicas: Resposta Hormonal ao Estresse Cirúrgico e Trauma
A resposta fisiológica ao estresse cirúrgico e ao trauma envolve uma série complexa de adaptações neuroendócrinas com significativas implicações clínicas no manejo do equilíbrio hidroeletrolítico. A compreensão detalhada da ativação de sistemas hormonais como o Sistema Renina-Angiotensina-Aldosterona (SRAA) e da liberação de hormônios como a Aldosterona e o Hormônio Antidiurético (ADH ou Vasopressina) é fundamental para a prática clínica.
Situações de estresse, como cirurgias ou traumas, frequentemente cursam com diminuição do volume sanguíneo ou da pressão arterial, seja por perda de fluidos ou por outros fatores relacionados ao evento agudo. Esses eventos são potentes gatilhos para a ativação do SRAA. Em resposta à diminuição da perfusão renal ou do volume circulante, os rins liberam renina, enzima que inicia a cascata hormonal convertendo o angiotensinogênio plasmático em angiotensina I. Subsequentemente, a enzima conversora de angiotensina (ECA) converte a angiotensina I em angiotensina II, o principal peptídeo efetor do sistema.
A angiotensina II exerce múltiplos efeitos cruciais na resposta ao estresse: promove vasoconstrição arterial sistêmica, ajudando a manter ou elevar a pressão arterial, e estimula diretamente a secreção de aldosterona pelo córtex da glândula adrenal. Além disso, a angiotensina II estimula a sede, contribuindo para a restauração do volume.
A aldosterona, um hormônio mineralocorticoide, desempenha um papel central nas alterações eletrolíticas observadas no pós-operatório e no trauma. Atuando nos túbulos distais e ductos coletores renais, a aldosterona aumenta a reabsorção de sódio (Na+) e, por consequência osmótica, de água, ao mesmo tempo que promove a secreção (excreção) de potássio (K+) e de íons hidrogênio (H+). Esta ação explica a fase inicial frequentemente observada após cirurgias, caracterizada pela retenção de sódio e água (resultando em aumento do volume sanguíneo) e pela perda de potássio, impactando o balanço eletrolítico do paciente. A regulação da aldosterona é influenciada tanto pelo SRAA quanto pela concentração plasmática de potássio.
Paralelamente, a diminuição do volume sanguíneo, o aumento da osmolaridade plasmática e a ativação do sistema nervoso simpático, condições comuns no trauma e no estresse cirúrgico de grande porte, estimulam a liberação de ADH (Vasopressina) pela neurohipófise (hipófise posterior). O ADH atua nos túbulos coletores renais, aumentando sua permeabilidade à água através da regulação de canais específicos (aquaporinas). Isso intensifica a reabsorção de água livre de solutos de volta para a circulação. O resultado é a produção de um menor volume de urina mais concentrada (refletido por um aumento na densidade urinária) e a conservação da água corporal, ajudando a manter o volume sanguíneo e a osmolaridade plasmática. Em concentrações elevadas, a vasopressina também pode exercer efeito vasoconstritor, contribuindo para a elevação da pressão arterial.
Em suma, a resposta hormonal coordenada ao estresse cirúrgico e ao trauma, mediada principalmente pela ativação integrada do SRAA (levando à produção de angiotensina II e aldosterona) e pela liberação de ADH, visa preservar o volume intravascular e a perfusão tecidual. Clinicamente, isso se manifesta como retenção de sódio e água e vasoconstrição, mas também acarreta alterações eletrolíticas importantes, como a depleção de potássio. O reconhecimento e a compreensão desses mecanismos são essenciais para o manejo hidroeletrolítico adequado de pacientes em situações de estresse agudo.
Densidade Urinária como Ferramenta de Avaliação do Equilíbrio Hídrico
A densidade urinária é um parâmetro laboratorial essencial que reflete a concentração de solutos dissolvidos na urina. Funciona como um indicador direto da capacidade renal em ajustar a excreção de água, ou seja, de concentrar ou diluir a urina para manter a homeostase hídrica e osmótica do organismo. A sua magnitude é determinada pela relação entre a massa de solutos excretados (principalmente eletrólitos como sódio e potássio, além de ureia e creatinina) e o volume de água em que estão diluídos.
A faixa de normalidade para a densidade urinária varia tipicamente entre 1.005 e 1.030 g/mL. A interpretação clínica desses valores é crucial para avaliar o estado de hidratação e a função tubular renal:
- Valores Elevados (acima de 1.030 g/mL): Indicam urina concentrada. Esta condição é frequentemente observada em estados de depleção de volume ou desidratação. Fisiologicamente, a redução do volume sanguíneo ou o aumento da osmolaridade plasmática estimulam a liberação do hormônio antidiurético (ADH), também conhecido como vasopressina. O ADH atua nos túbulos coletores renais, aumentando a reabsorção de água e, consequentemente, diminuindo o volume urinário e elevando a concentração de solutos e a densidade urinária.
- Valores Diminuídos (abaixo de 1.005 g/mL): Sugerem urina diluída. Esta situação pode ocorrer em resposta a uma sobrecarga hídrica (excesso de hidratação), onde a secreção de ADH é suprimida para facilitar a excreção do excesso de água. Também pode ser um sinal de condições patológicas como o diabetes insipidus, caracterizado por uma deficiência na secreção ou na resposta renal ao ADH, resultando na incapacidade de concentrar a urina adequadamente.
Dessa forma, a mensuração da densidade urinária oferece uma ferramenta diagnóstica e de monitoramento valiosa na avaliação do equilíbrio hídrico e da integridade da função renal de concentração e diluição.
Conclusão
A regulação hormonal do equilíbrio hidroeletrolítico é um processo complexo e vital, orquestrado por hormônios como o ADH e a aldosterona, sob a influência do SRAA. Esses sistemas trabalham em conjunto para manter a homeostase em diversas condições, incluindo o estresse cirúrgico e o trauma. A densidade urinária se apresenta como uma ferramenta valiosa na avaliação do estado de hidratação e da função renal. A compreensão desses mecanismos é essencial para o manejo clínico adequado e para garantir a saúde e o bem-estar dos pacientes.