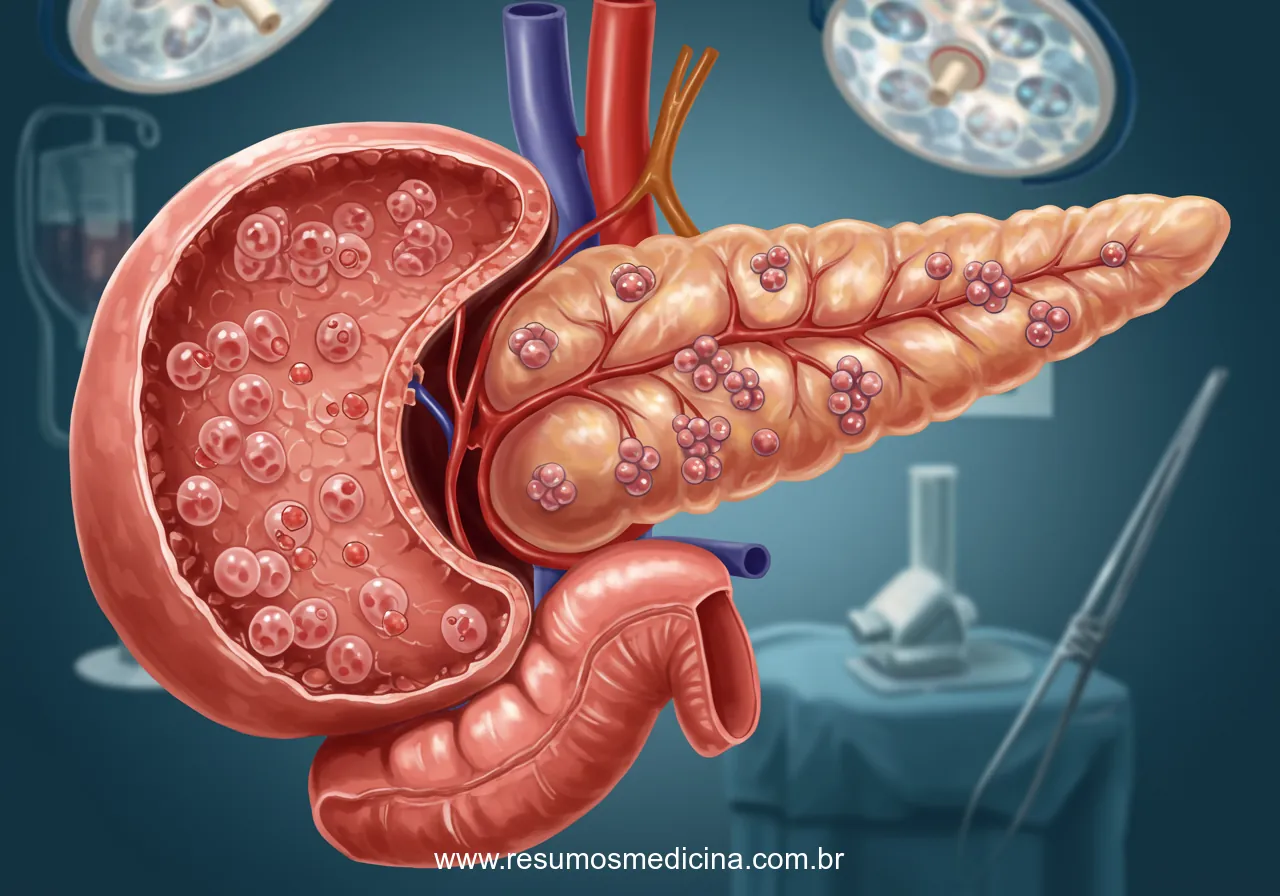
As lesões císticas do pâncreas (LCPs) representam um grupo diversificado de achados clínicos e patológicos, cuja identificação e caracterização precisas são essenciais para o direcionamento terapêutico. A heterogeneidade dessas lesões reside, principalmente, no seu potencial de malignidade, que varia desde condições benignas a neoplasias com risco significativo de transformação ou já estabelecidas como carcinomas invasivos. Portanto, compreender a classificação dessas lesões é fundamental para a prática oncológica.
Introdução e Classificação Geral das Lesões Císticas Pancreáticas
As LCPs são amplamente categorizadas em três grupos principais com base na sua etiologia e natureza histopatológica. A primeira categoria são as Coleções Fluidas Inflamatórias, cujo protótipo é o pseudocisto pancreático; estas são formações não neoplásicas, desprovidas de revestimento epitelial verdadeiro, encapsuladas por tecido fibroso ou de granulação, ricas em enzimas pancreáticas e frequentemente secundárias a episódios de pancreatite aguda, crônica ou trauma. A segunda categoria engloba os Cistos Não Neoplásicos, que incluem cistos verdadeiros com revestimento epitelial, mas sem potencial neoplásico inerente, como cistos de retenção, cistos linfoepiteliais e cistos de duplicação. A terceira e mais relevante categoria do ponto de vista oncológico são as Neoplasias Císticas Pancreáticas (NCPs), que são verdadeiros tumores com revestimento epitelial e potencial variável de malignização. A classificação da Organização Mundial da Saúde (OMS) é frequentemente utilizada para categorizar essas neoplasias, sendo crucial para a avaliação de risco e planejamento terapêutico.
Principais Tipos de Neoplasias Císticas Pancreáticas (NCPs)
- Neoplasia Cística Serosa (NCS) / Cistoadenoma Seroso (CAS): Tipicamente benigna, frequentemente apresentando um padrão microcístico com aspecto em ‘favo de mel’ à imagem. Possui risco de malignização considerado muito baixo ou desprezível.
- Neoplasia Mucinosa Cística (NMC) / Cistoadenoma Mucinoso: Considerada uma lesão pré-maligna ou com potencial inerente de malignização. Ocorre quase exclusivamente em mulheres, localiza-se classicamente no corpo e cauda do pâncreas, não se comunica com o sistema ductal e histologicamente apresenta um estroma do tipo ovariano subjacente ao epitélio mucinoso.
- Neoplasia Mucinosa Papilar Intraductal (NMPI ou IPMN): Origina-se no epitélio dos ductos pancreáticos (principal, ramos secundários ou ambos – tipo misto), caracterizada pela produção de mucina e crescimento papilar. Apresenta risco significativo e variável de progressão para carcinoma invasivo, sendo o envolvimento do ducto principal um fator de maior risco.
- Neoplasia Sólida Pseudopapilar (NSPP) / Tumor Sólido Pseudopapilar (TSP) ou Tumor de Frantz: Uma neoplasia rara, que acomete predominantemente mulheres jovens. Apresenta baixo potencial de malignidade e caracteriza-se por um padrão misto sólido-cístico com áreas de hemorragia ou necrose.
Neoplasia Cística Serosa (NCS) ou Cistoadenoma Seroso (CAS)
A Neoplasia Cística Serosa (NCS), ou Cistoadenoma Seroso (CAS), é uma lesão cística pancreática não mucinosa, caracterizada predominantemente por seu comportamento benigno. Epidemiologicamente, demonstra predileção pelo sexo feminino, sendo mais frequente em mulheres idosas. Frequentemente, é assintomática e descoberta incidentalmente durante exames de imagem realizados por outros motivos. A sua localização pode ocorrer em qualquer segmento do pâncreas (cabeça, corpo ou cauda).
Características Diagnósticas
O diagnóstico da NCS/CAS baseia-se primordialmente em achados de imagem e análise do fluido cístico quando disponível.
- Achados de Imagem (TC, RM, Ecoendoscopia): A morfologia mais clássica é a microcística, composta por múltiplos pequenos cistos que conferem um aspecto em “favo de mel” (honeycomb). Existe também a variante macrocística, com um número menor de cistos de maiores dimensões. A lesão é tipicamente bem delimitada por uma cápsula fibrosa. Um achado característico, embora não universal, é a presença de uma cicatriz central, por vezes com calcificações. A Ecoendoscopia (USE) pode fornecer detalhes morfológicos adicionais. Um aspecto crucial é a ausência de comunicação com o sistema ductal pancreático principal ou secundário.
- Análise do Fluido Cístico (via PAAF guiada por USE): A análise bioquímica do conteúdo cístico revela, caracteristicamente, níveis baixos ou indetectáveis do Antígeno Carcinoembrionário (CEA) e baixos níveis de amilase, refletindo a ausência de comunicação ductal. A mucina está tipicamente ausente no fluido.
- Aspectos Moleculares: Algumas NCS/CAS estão associadas a mutações somáticas no gene supressor de tumor VHL (von Hippel-Lindau).
Abordagem Terapêutica e Prognóstico
Dado o risco de malignização considerado muito baixo ou desprezível, a abordagem padrão para NCS/CAS assintomáticas é conservadora, consistindo em vigilância ativa (manejo expectante) com seguimento por imagem. A ressecção cirúrgica fica reservada para casos selecionados: pacientes sintomáticos (com dor abdominal, icterícia obstrutiva por compressão, etc.), situações onde persiste incerteza diagnóstica significativa em relação a outras neoplasias com potencial maligno, ou quando há crescimento documentado da lesão durante o período de acompanhamento. O prognóstico para pacientes com NCS/CAS é, em geral, excelente.
Neoplasia Mucinosa Cística (NMC) ou Cistoadenoma Mucinoso
A Neoplasia Mucinosa Cística (NMC), ou Cistoadenoma Mucinoso, é uma neoplasia cística pancreática classificada como mucinosa e reconhecida pelo seu potencial pré-maligno inerente. Sua epidemiologia é marcadamente distinta, acometendo quase exclusivamente o sexo feminino, com pico de incidência geralmente a partir da quarta ou quinta década de vida. Anatomicamente, localiza-se preferencialmente no corpo e/ou cauda do pâncreas.
Características Morfológicas e Histopatológicas
Morfologicamente, as NMCs são tipicamente lesões macrocísticas (usualmente > 2 cm), podendo ser uniloculares ou multiloculares, com septações e paredes bem definidas. Calcificações periféricas ou centrípetas podem ocorrer ocasionalmente. Histologicamente, a NMC é definida por um revestimento epitelial colunar produtor de mucina e, crucialmente, pela presença de um estroma subjacente do tipo ovariano (ovariano-like). Este estroma é considerado patognomônico e essencial para o diagnóstico diferencial, distinguindo a NMC de outras neoplasias císticas, em particular da NMPI. A classificação histológica inclui a avaliação do grau de displasia epitelial (baixo a alto grau), que se correlaciona diretamente com o risco de progressão para carcinoma invasivo. Uma característica fundamental é a ausência de comunicação entre a cavidade cística e o sistema ductal pancreático principal.
Achados Diagnósticos Complementares
A análise do fluido cístico, obtido por punção aspirativa guiada por ecoendoscopia, geralmente revela níveis elevados de Antígeno Carcinoembrionário (CEA) e presença de mucina, consistente com a natureza da lesão. Os níveis de amilase no fluido são caracteristicamente baixos, refletindo a falta de comunicação ductal. Imuno-histoquimicamente, o epitélio pode expressar marcadores como queratinas, CEA e CA 19-9, embora estes não sejam específicos da NMC.
Apresentação Clínica e Potencial de Malignidade
Muitas NMCs são assintomáticas e descobertas incidentalmente. Quando sintomáticas, podem causar dor abdominal vaga, massa palpável ou episódios de pancreatite. Sintomas mais graves como icterícia ou perda ponderal podem ocorrer em casos avançados ou de grandes dimensões com compressão extrínseca. O risco de transformação maligna (progressão para carcinoma invasivo) é significativo, estimado entre 10% e 30%. Fatores associados a maior risco incluem dimensões do cisto > 3 cm, presença de nódulos murais evidenciados em exames de imagem, espessamento da parede cística e presença de sintomatologia atribuível à lesão.
Abordagem Terapêutica
Dado o risco substancial de malignização, a ressecção cirúrgica é o tratamento padrão recomendado para a NMC. Para lesões situadas no corpo e/ou cauda pancreática, o procedimento habitual é a pancreatectomia distal (corpo-caudal), frequentemente associada à esplenectomia. A indicação cirúrgica é fortalecida em pacientes sintomáticos, com características radiológicas de alto risco ou em indivíduos com condições clínicas adequadas para o procedimento. A vigilância ativa pode ser considerada apenas em casos muito selecionados de pacientes de alto risco cirúrgico com lesões pequenas e sem características preocupantes, mas a ressecção permanece como a abordagem potencialmente curativa e preventiva da progressão para carcinoma invasivo.
Neoplasia Mucinosa Papilar Intraductal (NMPI ou IPMN)
A Neoplasia Mucinosa Papilar Intraductal (NMPI ou IPMN) é definida pelo crescimento papilar de células epiteliais produtoras de mucina que se originam e proliferam no interior do sistema ductal pancreático. Diferentemente da Neoplasia Cística Mucinosa (NCM) que acomete quase exclusivamente mulheres, a NMPI pode ocorrer em ambos os sexos e manifesta-se frequentemente em faixas etárias mais avançadas.
Classificação e Localização
A classificação da NMPI é fundamental para a estratificação de risco e baseia-se no segmento ductal pancreático envolvido:
- NMPI de Ducto Principal (NMPI-DP ou MD-IPMN): Caracterizada pelo envolvimento do ducto pancreático principal (DPP).
- NMPI de Ramos Laterais (NMPI-RL ou BD-IPMN): Afeta exclusivamente os ductos secundários ou ramos laterais.
- NMPI Mista (NMPI-M): Apresenta envolvimento concomitante do ducto principal e de ramos laterais.
Embora possa ocorrer em qualquer segmento pancreático, a NMPI localiza-se mais frequentemente na cabeça do pâncreas. O envolvimento do ducto principal (presente nas formas NMPI-DP e NMPI-M) associa-se a um risco significativamente maior de malignidade em comparação com a NMPI-RL pura.
Características Clínicas e Diagnósticas
Uma característica fundamental da NMPI é a sua comunicação direta com o sistema ductal pancreático. A produção excessiva de mucina pode levar à dilatação visível dos ductos acometidos e, eventualmente, à atrofia do parênquima pancreático adjacente. A apresentação clínica é variável: muitos casos são assintomáticos e descobertos incidentalmente. Quando sintomática, pode manifestar-se por dor abdominal, episódios recorrentes de pancreatite aguda (desencadeados pela obstrução ductal por tampões de mucina), diarreia ou sinais obstrutivos como icterícia (por compressão do ducto biliar ou envolvimento papilar). A observação endoscópica de saída de muco espesso pelo orifício papilar é um sinal clínico sugestivo.
A investigação diagnóstica apoia-se em exames de imagem como Tomografia Computadorizada (TC) e Ressonância Magnética (RM) com Colangiopancreatorressonância (CPRM), esta última oferecendo melhor detalhamento da arquitetura cística e da relação com os ductos. A Ecoendoscopia (USE) proporciona avaliação morfológica de alta resolução, permitindo identificar características de risco e guiar a Punção Aspirativa por Agulha Fina (PAAF). A análise do fluido cístico da NMPI tipicamente revela níveis elevados de amilase (reflexo da comunicação ductal) e do Antígeno Carcinoembrionário (CEA), juntamente com a presença de mucina. A citologia do aspirado pode identificar células displásicas ou malignas.
Risco de Malignidade e Fatores Associados (“High-Risk Stigmata” e “Worrisome Features”)
A NMPI possui um espectro de potencial de malignidade, desde displasia de baixo grau até carcinoma invasivo. O risco é estratificado com base em critérios clínicos e radiológicos, frequentemente categorizados conforme as diretrizes de consenso (ex: Fukuoka):
- Estigmas de Alto Risco (High-Risk Stigmata – HRS): Indicam elevada probabilidade de malignidade (displasia de alto grau ou carcinoma invasivo). Incluem: icterícia obstrutiva em paciente com lesão cística na cabeça pancreática; identificação de componente sólido (nódulo mural) > 5 mm com realce pós-contraste; dilatação do ducto pancreático principal (DPP) ≥ 10 mm; citologia suspeita ou positiva para malignidade.
- Características Preocupantes (Worrisome Features – WF): Sinalizam um risco aumentado de malignidade e geralmente indicam a necessidade de investigação adicional (ex: USE com PAAF se ainda não realizada) ou podem influenciar a decisão terapêutica. Incluem: dilatação do DPP entre 5 e 9 mm; presença de nódulo mural < 5 mm; tamanho do cisto ≥ 3 cm; paredes císticas espessadas ou com realce; dor abdominal de início recente ou alteração de padrão; alteração abrupta do calibre do DPP associada à atrofia pancreática distal.
Abordagem Terapêutica e Manejo
O manejo da NMPI requer uma decisão individualizada, preferencialmente em contexto multidisciplinar, baseada na estratificação de risco:
- Ressecção Cirúrgica: É geralmente indicada para todas as NMPI-DP e NMPI-M, devido ao seu risco intrínseco elevado. Também se recomenda para NMPI-RL que apresentem HRS ou WF significativas, além das lesões sintomáticas. O tipo de procedimento cirúrgico (duodenopancreatectomia, pancreatectomia distal, pancreatectomia total) depende da extensão e localização da lesão.
- Vigilância Ativa: Constitui uma opção para NMPI-RL assintomáticas, com diâmetro < 3 cm e sem HRS ou WF. A vigilância consiste em seguimento com exames de imagem periódicos (RM/CPRM ou TC, por vezes alternados ou complementados com USE) para monitorar o tamanho da lesão, o calibre do DPP e o surgimento de características de risco, seguindo protocolos específicos de intervalo e duração. Qualquer desenvolvimento de HRS ou WF relevantes durante o seguimento pode indicar a necessidade de reavaliação e potencial ressecção cirúrgica.
Neoplasia Sólida Pseudopapilar (NSPP) ou Tumor de Frantz (TSPP)
A Neoplasia Sólida Pseudopapilar (NSPP), também conhecida como Tumor de Frantz (TSPP), constitui uma entidade neoplásica pancreática rara, de natureza predominantemente sólido-cística. Apresenta uma marcada predileção pelo sexo feminino, incidindo tipicamente em mulheres jovens (geralmente antes dos 40 anos de idade). A localização mais frequente é no corpo e, especialmente, na cauda do pâncreas.
Caracteriza-se por um comportamento biológico majoritariamente indolente, sendo classificada como uma neoplasia de baixo grau ou baixo potencial de malignidade. O potencial metastático é considerado baixo, frequentemente estimado em menos de 5%. No entanto, é importante notar que casos com comportamento mais agressivo podem ocorrer.
Apresentação Clínica e Diagnóstico por Imagem
A NSPP é muitas vezes diagnosticada incidentalmente durante exames de imagem realizados por outras indicações. Quando sintomática, as manifestações clínicas costumam ser inespecíficas, como dor abdominal vaga ou sintomas decorrentes do efeito de massa da lesão sobre estruturas adjacentes. A investigação por imagem, através de Tomografia Computadorizada (TC) e Ressonância Magnética (RM), é fundamental para a caracterização. Os achados típicos incluem:
- Morfologia Geral: Massa bem delimitada, frequentemente encapsulada (com cápsula espessa) e de contornos regulares.
- Padrão Interno: Aspecto heterogêneo com um padrão misto, contendo componentes sólidos e císticos. A presença de áreas internas de hemorragia e necrose é comum e contribui significativamente para a aparência cística.
- Outros Achados: Calcificações ou septações internas podem estar presentes na lesão.
Características Histopatológicas e Imunohistoquímicas
Histologicamente, a NSPP exibe um padrão arquitetural distintivo, descrito como sólido-pseudopapilar. A avaliação imuno-histoquímica é crucial e demonstra, caracteristicamente, expressão nuclear/citoplasmática de beta-catenina. Adicionalmente, é frequente a expressão de receptores hormonais de estrogênio e progesterona, um achado que pode estar correlacionado com a predominância da neoplasia no sexo feminino.
Tratamento e Prognóstico
O tratamento padrão-ouro para a NSPP é a ressecção cirúrgica completa da lesão, que na maioria dos casos é curativa. Para tumores localizados no corpo ou cauda do pâncreas, o procedimento cirúrgico habitualmente indicado é a pancreatectomia distal (corpo-caudal), associada à linfadenectomia regional e esplenectomia. Em casos raros de doença metastática, terapias adjuvantes, como quimioterapia ou terapia direcionada, podem ser consideradas.
O prognóstico para pacientes com NSPP submetidos à ressecção cirúrgica completa é, em geral, excelente, com elevadas taxas de sobrevida a longo prazo. A ocorrência de recorrência local ou metástases à distância é infrequente, mas possível, justificando a recomendação de acompanhamento pós-operatório regular para vigilância.
Diagnóstico Diferencial e Pseudocistos Pancreáticos
A diferenciação precisa entre as Neoplasias Císticas Pancreáticas (NCPs) e as lesões não neoplásicas, particularmente o pseudocisto pancreático, é um passo diagnóstico de fundamental importância clínica. As implicações prognósticas e as abordagens terapêuticas são substancialmente distintas, tornando a correta identificação da natureza da lesão cística um fator determinante no manejo do paciente.
Caracterização Distintiva do Pseudocisto Pancreático
O pseudocisto pancreático, ao contrário das NCPs, não é uma neoplasia verdadeira, mas sim uma coleção fluida de natureza inflamatória. Sua formação é classicamente uma sequela de pancreatite (aguda ou crônica) ou trauma pancreático, manifestando-se tipicamente 4 a 6 semanas após o evento inicial. Os fatores de risco para o desenvolvimento de pseudocistos espelham aqueles associados à pancreatite, como o consumo de álcool e a presença de cálculos biliares. A principal característica histopatológica que o distingue das neoplasias é a ausência de um revestimento epitelial; sua parede é constituída por tecido de granulação ou fibroso.
A análise bioquímica do conteúdo líquido aspirado de um pseudocisto revela, caracteristicamente, níveis elevados de enzimas pancreáticas (amilase e lipase) e, crucialmente para o diagnóstico diferencial, níveis baixos de Antígeno Carcinoembrionário (CEA), contrastando com os níveis frequentemente elevados encontrados em neoplasias mucinosas (NMC e NMPI).
Clinicamente, pseudocistos podem ser assintomáticos ou manifestar-se com dor abdominal, presença de massa palpável (frequentemente no hipocôndrio esquerdo), náuseas, vômitos e sensação de empachamento pós-prandial.
Implicações na Conduta Clínica
A diferenciação entre estas entidades baseia-se na integração de múltiplos fatores: o contexto clínico (história de pancreatite), os achados morfológicos em exames de imagem, a análise bioquímica do fluido cístico (níveis de CEA e amilase) e a ausência de potencial intrínseco de malignização no caso dos pseudocistos. Enquanto as NCPs, em particular as mucinosas (NMC e NMPI), carregam um risco inerente de transformação maligna, os pseudocistos são lesões benignas por natureza.
Esta distinção direciona o planejamento terapêutico: o manejo dos pseudocistos é primariamente guiado pela presença e severidade dos sintomas ou pelo desenvolvimento de complicações (como infecção, ruptura ou sangramento), variando desde a observação expectante até a necessidade de drenagem (endoscópica, percutânea ou cirúrgica). Em contraste, a abordagem das NCPs é estratificada pelo risco de malignidade, determinado pelas características da lesão (tipo histológico suspeito, tamanho, presença de nódulos murais, dilatação ductal), podendo variar entre vigilância ativa com seguimento imagiológico rigoroso e a ressecção cirúrgica com intenção curativa e oncológica.
Abordagem Diagnóstica: Imagem e Análise do Fluido Cístico
A investigação diagnóstica das lesões císticas pancreáticas fundamenta-se em um arsenal de modalidades de imagem e na análise bioquímica e citológica do fluido cístico, quando obtido. Esta abordagem combinada é crucial para a caracterização precisa da lesão, estratificação do risco de malignidade e definição da conduta terapêutica subsequente.
Modalidades de Imagem
As técnicas de imagem são essenciais na avaliação inicial e no seguimento das lesões císticas pancreáticas, fornecendo informações detalhadas sobre tamanho, localização, características morfológicas (parede, septações, componente sólido/nódulos murais) e a relação da lesão com o sistema ductal pancreático.
- Tomografia Computadorizada (TC): A TC multidetectores com contraste é frequentemente utilizada na avaliação inicial. É particularmente útil para determinar o tamanho e a localização precisa da lesão, detectar calcificações (que podem sugerir diagnósticos específicos, como a cicatriz central ocasional na NCS ou calcificações periféricas na NMC), e avaliar o envolvimento ou compressão de estruturas vasculares adjacentes.
- Ressonância Magnética (RM) com Colangiopancreatorressonância (CPRM): A RM, especialmente quando combinada com sequências de CPRM, oferece caracterização tecidual superior à TC. Permite uma avaliação detalhada do conteúdo interno dos cistos, da presença e complexidade de septações, e é mais sensível na identificação de nódulos murais ou componentes sólidos. Fundamentalmente, a CPRM demonstra com maior acurácia a presença ou ausência de comunicação entre a lesão cística e o ducto pancreático principal (DPP) ou seus ramos, informação vital na caracterização das IPMNs e na diferenciação de pseudocistos.
- Ultrassonografia Endoscópica (USE / Ecoendoscopia): A USE é considerada o método de imagem com maior resolução espacial para o estudo morfológico detalhado das lesões císticas pancreáticas. Permite uma avaliação minuciosa da parede do cisto, de septos internos finos e a detecção de pequenos nódulos murais (<5 mm) ou componentes sólidos que podem não ser visíveis em TC ou RM. Além da avaliação morfológica superior, a USE desempenha um papel central ao guiar, com precisão e segurança, a Punção Aspirativa por Agulha Fina (PAAF) para obtenção de fluido cístico e/ou material para análise citológica/histológica.
Análise do Fluido Cístico por PAAF
A PAAF guiada por USE permite a coleta de fluido cístico para análise laboratorial, fornecendo informações bioquímicas, enzimáticas, de marcadores tumorais e citológicas que complementam significativamente os achados de imagem e são de grande valor no diagnóstico diferencial e na avaliação do potencial de malignidade.
- Análises Realizadas: Os principais componentes analisados no fluido cístico incluem a dosagem de marcadores tumorais, como o Antígeno Carcinoembrionário (CEA) e o Carboidrato Antígeno 19-9 (CA 19-9), a determinação dos níveis da enzima amilase, a verificação da presença ou ausência de mucina e a análise citológica.
- Citologia: A análise citológica busca identificar a presença de células epiteliais, avaliar atipias e detectar células francamente malignas. Um resultado positivo para malignidade ou displasia de alto grau possui alto valor preditivo positivo e confirma a natureza agressiva da lesão. Contudo, é importante reconhecer que a sensibilidade da citologia para detectar malignidade em lesões císticas pode ser limitada, variando conforme o tipo de lesão e a celularidade da amostra. Um resultado negativo ou inconclusivo não exclui a possibilidade de malignidade ou de lesão pré-maligna, devendo sempre ser interpretado em conjunto com os achados clínicos, de imagem e dos marcadores bioquímicos do fluido.
A integração criteriosa dos dados clínicos, dos achados detalhados das diferentes modalidades de imagem e dos resultados da análise do fluido cístico (quando realizada) permite a classificação mais precisa da lesão cística pancreática, a estratificação do risco individualizado de malignidade e, consequentemente, a definição da estratégia de manejo mais apropriada para cada paciente, seja ela vigilância ativa ou ressecção cirúrgica.
Avaliação de Risco, Manejo e Indicações Cirúrgicas nas Neoplasias Císticas Pancreáticas
A conduta frente a uma neoplasia cística pancreática (NCP) é direcionada por uma criteriosa estratificação do risco de malignidade. Esta avaliação é fundamental para determinar a estratégia de manejo mais adequada, que oscila entre a vigilância ativa e a ressecção cirúrgica, influenciando diretamente o prognóstico do paciente.
Estratificação do Risco de Malignidade
A estimativa do risco de malignidade associado a uma NCP baseia-se na integração de múltiplos fatores clínicos, radiológicos e, quando aplicável, citopatológicos. A presença de um ou mais dos seguintes elementos eleva a suspeita de transformação maligna ou de malignidade já estabelecida:
- Tipo Histológico Suspeito: Certos tipos, como a Neoplasia Mucinosa Cística (NMC) e a Neoplasia Mucinosa Papilar Intraductal do ducto principal (NMPI-DP) ou Mista, carregam um risco inerentemente mais elevado em comparação com o Cistoadenoma Seroso (NCS) ou a maioria das NMPIs de ramo lateral (NMPI-RL) puras.
- Dimensões da Lesão: Cistos com diâmetro superior a 3 cm (30 mm).
- Componente Sólido ou Nódulos Murais: A identificação de componente sólido intralesional ou de nódulos na parede do cisto, particularmente se maiores que 5 mm e com realce após administração de contraste intravenoso.
- Dilatação do Ducto Pancreático Principal (DPP): Dilatação considerada de alto risco (≥ 10 mm) ou preocupante (5-9 mm, ou >1 cm em algumas referências).
- Características da Parede Cística: Espessamento significativo ou realce anômalo da parede do cisto.
- Crescimento da Lesão: Aumento rápido ou progressivo do tamanho da lesão documentado em exames de imagem seriados.
- Sintomatologia Relacionada: O surgimento de sintomas atribuíveis à lesão, como dor abdominal de início recente, icterícia obstrutiva ou episódios de pancreatite.
- Achados da Punção Aspirativa por Agulha Fina (PAAF): Citologia suspeita ou positiva para malignidade/displasia de alto grau; níveis elevados de CEA no líquido cístico são altamente sugestivos de neoplasias mucinosas (NMC, NMPI) e influenciam a abordagem.
- Suspeita de Invasão Ductal: Evidência radiológica ou endoscópica de invasão do ducto pancreático ou biliar.
Estratégias de Manejo
Com base na estratificação de risco, o manejo individualizado compreende duas abordagens principais:
- Vigilância Ativa: Reservada para lesões consideradas de baixo risco de malignidade, como NCS assintomáticas ou NMPI-RL pequenas sem características de risco. Consiste em acompanhamento clínico e imagiológico periódico (TC, RM/CPRM ou USE) para monitorar estabilidade ou surgimento de alterações suspeitas. Os protocolos e intervalos de seguimento variam conforme as diretrizes atuais e as características específicas da lesão e do paciente.
- Ressecção Cirúrgica: Considerada o tratamento padrão para lesões com alto risco ou suspeita de malignidade, lesões sintomáticas, ou para tipos específicos de NCP com potencial maligno intrínseco significativo.
Indicações para Ressecção Cirúrgica
A intervenção cirúrgica é formalmente indicada nas seguintes situações, após avaliação criteriosa do risco-benefício:
- Presença de sintomas clínicos claramente atribuíveis à NCP (dor, icterícia, pancreatite, etc.).
- Diagnóstico confirmado ou forte suspeita de Neoplasia Mucinosa Cística (NMC).
- Diagnóstico confirmado ou forte suspeita de Neoplasia Sólida Pseudopapilar (NSPP / Tumor de Frantz).
- Diagnóstico de Neoplasia Mucinosa Papilar Intraductal do Ducto Principal (NMPI-DP) ou Mista.
- Diagnóstico de Neoplasia Mucinosa Papilar Intraductal de Ramo Lateral (NMPI-RL) que apresente ‘High-Risk Stigmata’ (ex: icterícia obstrutiva, nódulo mural >5mm com realce, DPP ≥10mm, citologia positiva) ou ‘Worrisome Features’ significativas (ex: cisto ≥3cm, nódulo mural <5mm, DPP 5-9mm, espessamento parietal, crescimento rápido, dor nova) que justifiquem a intervenção após avaliação complementar (frequentemente USE com PAAF).
- Lesões císticas indeterminadas com suspeita robusta de malignidade que não pôde ser afastada por métodos não invasivos ou minimamente invasivos.
- Presença de critérios de alto risco confirmados, como componente sólido > 30mm ou citologia positiva para malignidade.
Opções Cirúrgicas
A modalidade cirúrgica é selecionada com base na localização anatômica da lesão no pâncreas:
- Duodenopancreatectomia (Cirurgia de Whipple): Procedimento padrão para neoplasias localizadas na cabeça do pâncreas ou processo uncinado.
- Pancreatectomia Distal (Corpo-caudal): Indicada para lesões situadas no corpo ou na cauda pancreática. A associação com esplenectomia depende da proximidade da lesão ao hilo esplênico, do tipo histológico (ex: esplenectomia frequentemente associada na ressecção do Tumor de Frantz por razões oncológicas) e da possibilidade de preservação vascular.
A decisão terapêutica final, especialmente a indicação cirúrgica, deve ser sempre individualizada, ponderando o risco estimado de malignidade da lesão, os riscos inerentes ao procedimento cirúrgico, a expectativa de vida, as comorbidades e as preferências do paciente, idealmente discutida em ambiente multidisciplinar.