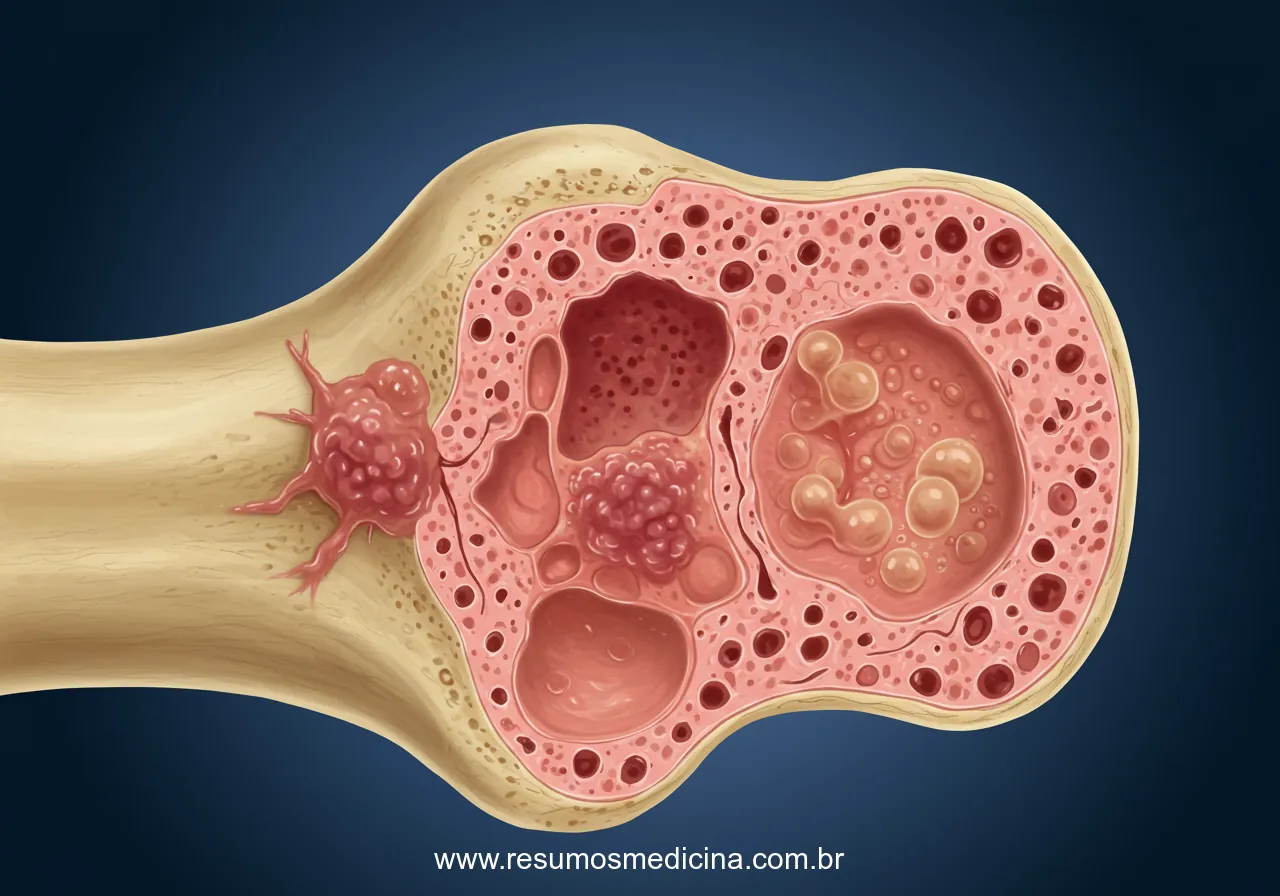
As metástases ósseas constituem uma complicação clinicamente significativa e prevalente em pacientes oncológicos, exercendo um impacto substancial no prognóstico e na qualidade de vida. Diversas neoplasias primárias exibem um notável tropismo pelo tecido ósseo, disseminando-se para o esqueleto através de vias e mecanismos específicos, com predileção por determinadas localizações anatômicas.
Introdução às Metástases Ósseas: Epidemiologia e Predileção Anatômica
A compreensão da epidemiologia das metástases ósseas é fundamental para a prática clínica. A propensão à metastização para o osso varia consideravelmente entre os tipos de câncer, sendo influenciada por características intrínsecas do tumor, pela complexa interação com o microambiente ósseo e pela resposta imune do hospedeiro.
Principais Neoplasias Primárias Associadas
Os tumores primários que mais frequentemente originam metástases ósseas incluem:
- Em mulheres: Câncer de mama (mais prevalente), pulmão, tireoide e rim.
- Em homens: Câncer de próstata (principal causa, frequentemente associado a lesões osteoblásticas devido à estimulação de osteoblastos), pulmão, rim e tireoide.
- Outros relevantes: O mieloma múltiplo, uma neoplasia hematológica primária da medula óssea, classicamente causa lesões osteolíticas e representa um importante diagnóstico diferencial. Cânceres de pulmão, rim, tireoide e mama frequentemente estão associados a lesões predominantemente osteolíticas (resultantes da ativação de osteoclastos).
É crucial notar que a frequência relativa e o padrão (lítico, blástico ou misto) podem variar conforme dados epidemiológicos, subtipo histológico e a população estudada.
Locais Esqueléticos Predominantes e Mecanismos de Predileção
A disseminação metastática para o esqueleto ocorre majoritariamente por via hematogênica, através da qual células tumorais circulantes alcançam e se instalam na medula óssea. A disseminação por via linfática é considerada menos comum. Observa-se uma acentuada predileção por sítios específicos do esqueleto:
- Coluna Vertebral
- Pelve
- Costelas
- Fêmur Proximal
- Úmero Proximal
Essa distribuição preferencial, notadamente no esqueleto axial e nas porções proximais dos ossos longos, é atribuída a múltiplos fatores inter-relacionados:
- Alta Vascularização da Medula Óssea Vermelha: Estas regiões possuem um rico suprimento sanguíneo sinusoidal, facilitando o acesso e a extravasamento das células tumorais.
- Fluxo Sanguíneo Lento e Preferencial: Padrões hemodinâmicos na medula óssea podem favorecer a retenção das células neoplásicas.
- Microambiente Ósseo Propício: A medula óssea é um nicho rico em fatores de crescimento, citocinas e moléculas de adesão que promovem a ancoragem (adesão), sobrevivência e proliferação das células tumorais metastáticas. A interação bidirecional entre as células tumorais e as células residentes do estroma ósseo (incluindo osteoblastos, osteoclastos e suas células precursoras) é determinante para o estabelecimento e a progressão das metástases, influenciando também o tipo de lesão óssea resultante (lítica ou blástica).
- Proximidade Anatômica: A proximidade de certos órgãos primários ao esqueleto axial pode influenciar os padrões de disseminação em alguns casos, embora a via hematogênica seja dominante.
O entendimento detalhado da epidemiologia, dos padrões de distribuição anatômica e dos mecanismos subjacentes à predileção óssea é essencial para a suspeição clínica precoce, o estadiamento preciso e o desenvolvimento de estratégias terapêuticas eficazes no manejo das metástases ósseas.
Vias de Disseminação e Mecanismos de Colonização Óssea
A chegada de células neoplásicas ao esqueleto ocorre majoritariamente pela via hematogênica. Neste processo complexo, células tumorais se desprendem do sítio primário, sobrevivem na circulação sanguínea e alcançam a microvasculatura da medula óssea. Embora menos frequente, a disseminação por via linfática também pode contribuir para o estabelecimento de metástases ósseas.
Contudo, a mera chegada das células tumorais ao ambiente ósseo não garante a formação de uma metástase clínica. O processo de colonização é fundamental e depende intrinsecamente da interação bidirecional entre as células neoplásicas e os componentes do microambiente ósseo, incluindo células estromais, matriz extracelular, osteoblastos e osteoclastos.
Mecanismos de Alteração Óssea Induzidos pela Colonização
A interação entre as células tumorais e o microambiente ósseo resulta na desregulação do processo normal de remodelação óssea, levando a padrões distintos de lesões metastáticas:
- Mecanismo Osteolítico: As células tumorais podem secretar fatores que estimulam direta ou indiretamente a ativação e a atividade dos osteoclastos. Isso resulta em um aumento da reabsorção óssea, levando à destruição do osso preexistente. Este mecanismo é frequentemente observado em metástases de carcinomas de mama, pulmão e mieloma múltiplo.
- Mecanismo Osteoblástico: Alternativamente, as células tumorais podem liberar fatores que estimulam a proliferação e a atividade dos osteoblastos. Isso leva à deposição de osso novo, frequentemente de forma desorganizada e estruturalmente frágil. Este padrão é característico, por exemplo, das metástases de câncer de próstata.
- Mecanismo Misto: Muitas metástases exibem características de ambos os processos, com áreas de destruição óssea coexistindo com áreas de formação óssea reacional.
Compreender estas vias de disseminação e, crucialmente, os mecanismos celulares e moleculares que governam a colonização e a subsequente alteração da homeostase óssea, é essencial para o desenvolvimento de estratégias terapêuticas direcionadas.
Classificação das Lesões Metastáticas Ósseas: Líticas, Blásticas e Mistas
As metástases ósseas são categorizadas com base nos seus padrões predominantes de alteração da estrutura óssea, os quais refletem os mecanismos biológicos subjacentes à interação entre as células neoplásicas e o microambiente ósseo. Esta classificação, fundamentalmente radiológica e patológica, divide as lesões em três tipos principais: osteolíticas (líticas), osteoblásticas (blásticas) e mistas.
Lesões Osteolíticas (Líticas)
Caracterizam-se pela destruição do tecido ósseo preexistente. O processo fisiopatológico central envolve a ativação exacerbada dos osteoclastos, células responsáveis pela reabsorção óssea, mediada por fatores secretados pelas células tumorais ou pelas células do estroma ósseo adjacente. Radiologicamente, as lesões líticas manifestam-se como áreas de diminuição da densidade óssea, aparecendo como zonas radiolucentes ou radiotransparentes. A consequência clínica direta é a fragilização estrutural do osso, aumentando o risco de fraturas patológicas e contribuindo para a dor óssea.
Lesões Osteoblásticas (Blásticas)
Definem-se pela formação excessiva e frequentemente desorganizada de osso novo. Neste tipo de lesão, as células metastáticas estimulam a atividade proliferativa e funcional dos osteoblastos, que depositam matriz óssea adicional. Contudo, esse novo osso é muitas vezes de natureza reativa, apresentando características estruturais anormais e sendo mecanicamente inferior ao osso lamelar saudável. Nos exames de imagem, as lesões blásticas são identificadas como áreas de aumento da densidade óssea, descritas como radiopacas ou escleróticas.
Lesões Mistas
Frequentemente, as metástases ósseas exibem características tanto do processo lítico quanto do blástico simultaneamente, sendo classificadas como mistas. Radiologicamente, estas lesões podem apresentar áreas de radiolucência (líticas) justapostas a áreas de radiopacidade (blásticas) dentro da mesma lesão ou em diferentes sítios metastáticos no mesmo paciente. É crucial reconhecer que esta classificação representa um espectro contínuo e não categorias estanques; a predominância de um padrão sobre o outro pode variar, e um mesmo tipo de tumor primário pode induzir diferentes respostas ósseas (lítica, blástica ou mista) em diferentes lesões ou momentos.
A correta caracterização do tipo de lesão metastática (lítica, blástica ou mista) possui relevância clínica, podendo auxiliar na investigação da possível origem do tumor primário desconhecido e na avaliação da resposta às terapias instituídas.
Fisiopatologia da Dor Óssea Associada a Metástases
A dor óssea representa uma manifestação clínica frequente e significativamente debilitante em pacientes com metástases ósseas. A compreensão dos seus mecanismos fisiopatológicos é fundamental para o manejo clínico adequado. A gênese da dor metastática óssea é multifatorial, envolvendo processos complexos que interligam as células tumorais, o microambiente ósseo e o sistema nervoso periférico.
Um dos principais mecanismos envolve a liberação de mediadores inflamatórios, tanto pelas células neoplásicas quanto pelas células estromais e imunes presentes no microambiente ósseo adjacente ao tumor. Esses mediadores, que incluem citocinas, quimiocinas e fatores de crescimento, atuam diretamente sobre as terminações nervosas livres (nociceptores) presentes no periósteo e no osso, promovendo a sua sensibilização. Este processo de sensibilização periférica reduz o limiar de disparo dos nociceptores e amplifica a resposta a estímulos nóxicos, resultando em hiperalgesia.
Adicionalmente, a própria destruição da arquitetura óssea, seja por atividade osteolítica predominante ou mesmo no contexto de formação óssea desorganizada (osteoblástica), contribui mecanicamente para a dor. A perda de integridade estrutural pode levar a microfraturas ou instabilidade, estimulando nociceptores mecânicos. Por fim, o crescimento expansivo da massa tumoral ou a deformidade óssea resultante podem levar à compressão direta de estruturas nervosas adjacentes, como raízes nervosas ou nervos periféricos, gerando dor neuropática associada.
Abordagem Diagnóstica por Imagem para Metástases Ósseas
A investigação e o diagnóstico das metástases ósseas fundamentam-se primordialmente na utilização de métodos de imagem. A seleção da modalidade apropriada é guiada pelo contexto clínico, pelas características suspeitas da lesão e pela necessidade de detalhamento anatômico ou avaliação da extensão da doença. Embora não seja um método de imagem, a biópsia óssea guiada por imagem frequentemente se faz necessária para a confirmação histopatológica definitiva e para determinar a histologia específica do tumor metastático.
Principais Métodos de Imagem
As técnicas de imagem desempenham papéis complementares na detecção, caracterização e estadiamento das lesões metastáticas no esqueleto:
- Radiografia Convencional (Raio-X): Frequentemente empregada como método inicial, a radiografia é útil para identificar alterações estruturais ósseas mais avançadas, como as lesões líticas e blásticas já estabelecidas (conforme classificadas anteriormente), e para avaliar a presença de fraturas patológicas. Contudo, apresenta sensibilidade limitada para a detecção de lesões precoces ou para a avaliação detalhada da infiltração da medula óssea.
- Cintilografia Óssea: Este método funcional destaca-se pela alta sensibilidade na detecção de áreas com atividade osteoblástica aumentada, característica da reação óssea à presença de metástases. É particularmente valiosa para o rastreamento de corpo inteiro, permitindo identificar lesões metabolicamente ativas, muitas vezes antes de serem visíveis radiograficamente. Sua principal limitação é a baixa especificidade, pois a captação aumentada do radiotraçador pode ocorrer em diversas outras condições ósseas (inflamatórias, traumáticas, degenerativas).
- Tomografia Computadorizada (TC): A TC fornece imagens seccionais de alta resolução espacial, oferecendo um detalhamento anatômico superior da estrutura óssea cortical e trabecular. É excelente para definir com precisão a morfologia das lesões (padrões lítico, blástico ou misto), avaliar a integridade cortical, o risco de fratura iminente, a extensão intraóssea da lesão e para guiar procedimentos percutâneos como biópsias.
- Ressonância Magnética (RM): A RM é a modalidade de escolha para a avaliação detalhada da medula óssea e das partes moles adjacentes. Sua alta resolução de contraste permite detectar precocemente a infiltração medular por células neoplásicas, mesmo antes do surgimento de alterações estruturais significativas. É fundamental na avaliação de potencial compressão de estruturas neurais, como a medula espinhal ou raízes nervosas (especialmente em metástases vertebrais), e na definição precisa da extensão extraóssea do tumor.
A seleção criteriosa e, frequentemente, a combinação dessas modalidades de imagem são essenciais para um diagnóstico preciso, estadiamento acurado da doença metastática óssea e para o planejamento terapêutico individualizado do paciente oncológico.
Diagnóstico Diferencial, Confirmação Histológica e Marcadores Bioquímicos
Após a suspeita ou identificação inicial de lesões ósseas por métodos de imagem, etapas diagnósticas complementares são frequentemente indispensáveis para a confirmação etiológica definitiva e para a avaliação metabólica da doença.
Confirmação por Biópsia Óssea
A análise histopatológica de uma amostra de tecido ósseo obtida por biópsia permanece como padrão-ouro para a confirmação de metástase óssea. Este procedimento é particularmente relevante em cenários onde os achados de imagem são atípicos ou inconclusivos, ou quando a identificação do sítio primário do tumor é necessária para definir a estratégia terapêutica mais adequada. A biópsia permite determinar a linhagem histológica das células neoplásicas presentes no osso, confirmando a natureza metastática.
Diagnóstico Diferencial de Lesões Ósseas
A interpretação de achados radiológicos, especialmente lesões com padrão osteolítico, requer uma abordagem sistemática para o diagnóstico diferencial. As principais etiologias a serem consideradas incluem metástases de carcinomas diversos, neoplasias hematológicas com envolvimento ósseo (como o mieloma múltiplo) e, com menor frequência, tumores ósseos primários. A diferenciação adequada exige a correlação criteriosa entre os dados clínicos do paciente, as características detalhadas da lesão nos diferentes exames de imagem e, em muitos casos, a confirmação histológica obtida por biópsia, sendo crucial para determinar a causa subjacente.
Marcadores Bioquímicos: Relevância da Fosfatase Alcalina
Marcadores bioquímicos séricos podem fornecer informações adicionais sobre a atividade metabólica óssea. A fosfatase alcalina (FA) total sérica é frequentemente avaliada neste contexto. Sua elevação pode indicar um aumento da atividade osteoblástica, seja como componente primário da metástase (lesões predominantemente blásticas ou mistas) ou como uma resposta osteoblástica reacional a lesões predominantemente líticas. Contudo, a FA sérica total carece de especificidade, pois níveis elevados também são encontrados em outras condições, notadamente em doenças hepatobiliares. A diferenciação das isoenzimas (óssea vs. hepática) pode auxiliar na interpretação. Na ausência de outras causas identificáveis, como doença hepática, uma elevação da isoenzima óssea da FA pode ser um indicador significativo de envolvimento esquelético ativo por doença metastática.