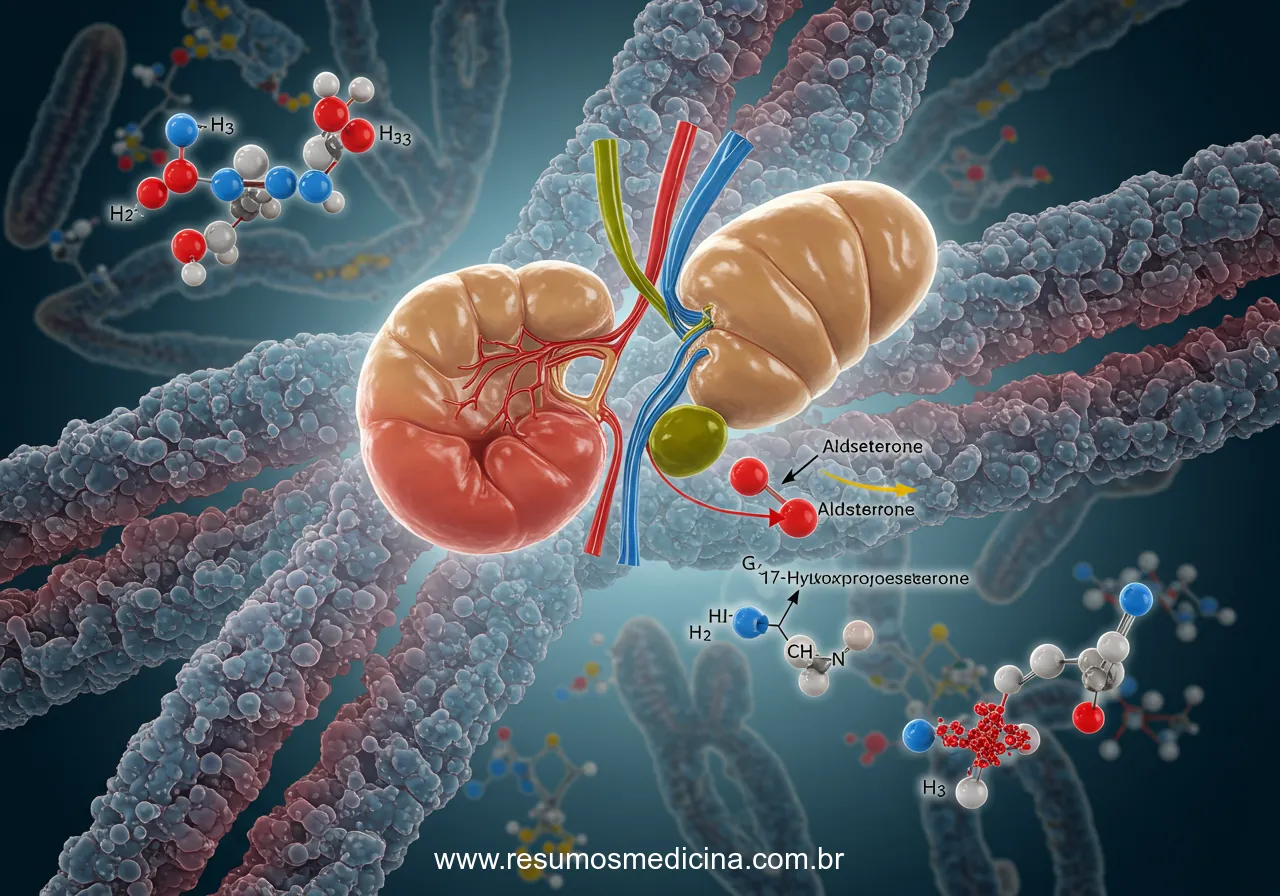
A Hiperplasia Adrenal Congênita (HAC) compreende um grupo de doenças autossômicas recessivas marcadas por falhas enzimáticas na via de produção dos esteroides adrenais. A forma mais comum, responsável por mais de 90% dos casos, surge da deficiência da enzima 21-hidroxilase. Este artigo explora o impacto da HAC na diferenciação sexual, desenvolvimento genital e suas manifestações clínicas, além de abordar o diagnóstico e as diferentes formas da doença, incluindo as manifestações sistêmicas e tardias.
Impacto Hormonal e Fisiopatologia da HAC
Fisiopatologicamente, o bloqueio enzimático na esteroidogênese adrenal leva à diminuição da produção de cortisol e, frequentemente, de aldosterona. A redução dos níveis de cortisol sérico estimula, por feedback negativo, um aumento na secreção do hormônio adrenocorticotrófico (ACTH) pela hipófise. Este aumento crônico de ACTH resulta em hiperplasia das glândulas adrenais, na tentativa de compensar a produção deficiente de cortisol. Contudo, o aumento do ACTH e o bloqueio enzimático levam ao acúmulo de precursores esteroides a montante do defeito, como a 17-hidroxiprogesterona (17-OHP) na deficiência de 21-hidroxilase. Esses precursores são então desviados para vias metabólicas alternativas, notadamente a síntese de andrógenos adrenais, como a testosterona.
As consequências clínicas da HAC derivam diretamente dessas alterações hormonais:
- Deficiência de Cortisol: Resulta em uma resposta inadequada ao estresse fisiológico, risco de hipoglicemia e pode contribuir para hipotensão, culminando potencialmente em crise adrenal (choque).
- Deficiência de Aldosterona: Compromete a capacidade renal de reabsorver sódio e excretar potássio nos túbulos distais. Isso leva à perda de sal, resultando em hiponatremia, hipercalemia, desidratação, hipovolemia e acidose metabólica. A hipercalemia severa representa risco significativo de arritmias cardíacas. A combinação dessas alterações configura a crise adrenal perdedora de sal, uma emergência médica neonatal.
- Excesso de Andrógenos: O aumento da produção de andrógenos tem efeitos virilizantes. Em indivíduos geneticamente femininos (46,XX), a exposição intrauterina a níveis elevados de andrógenos causa virilização da genitália externa, resultando em graus variáveis de ambiguidade genital ao nascimento (pseudo-hermafroditismo feminino). Em indivíduos geneticamente masculinos (46,XY), o excesso androgênico pode manifestar-se mais tardiamente com puberdade precoce ou, ao nascimento, com sinais sutis como aumento peniano ou hiperpigmentação escrotal.
Portanto, a HAC representa um distúrbio complexo com implicações significativas no equilíbrio hidroeletrolítico, na resposta ao estresse e no desenvolvimento sexual, exigindo diagnóstico e manejo adequados desde o período neonatal.
Embriologia da Diferenciação Sexual: Processo Normal
O desenvolvimento sexual durante o período embrionário é um processo complexo e sequencial, iniciado pela constituição cromossômica do concepto. A base para a diferenciação em fenótipo masculino ou feminino depende da presença ou ausência do cromossomo Y e da subsequente cascata hormonal.
Diferenciação Gonadal e dos Ductos Internos
Inicialmente, as gônadas são indiferenciadas. A presença do cromossomo Y, especificamente o gene SRY (fator determinante testicular), induz a diferenciação da gônada primitiva em testículo. Na ausência do cromossomo Y (constituição 46,XX), a gônada indiferenciada se desenvolve em ovário. Ambos os sexos possuem inicialmente os dois sistemas de ductos internos: os ductos de Müller (paramesonéfricos) e os ductos de Wolff (mesonéfricos).
No sexo masculino (46,XY), os testículos fetais começam a produzir dois hormônios cruciais: o Hormônio Anti-Mülleriano (AMH) e a testosterona. O AMH, produzido pelas células de Sertoli, induz a regressão completa dos ductos de Müller. A testosterona, produzida pelas células de Leydig, atua na estabilização e diferenciação dos ductos de Wolff, que originarão o epidídimo, o ducto deferente e as vesículas seminais.
No sexo feminino (46,XX), a ausência do fator SRY leva ao desenvolvimento ovariano. Como os ovários não produzem AMH significativo, os ductos de Müller persistem e se diferenciam para formar o útero, as trompas de Falópio e o terço superior da vagina. Na ausência de níveis elevados de testosterona, os ductos de Wolff regridem espontaneamente.
Diferenciação da Genitália Externa
A genitália externa também passa por um estágio inicial indiferenciado, comum a ambos os sexos, composta pelo tubérculo genital, pregas uretrais e protuberâncias labioescrotais (ou genitais). A diferenciação subsequente é primariamente dependente da presença ou ausência de andrógenos, especificamente a diidrotestosterona (DHT).
No sexo masculino, a testosterona produzida pelos testículos é convertida em DHT pela enzima 5α-redutase nos tecidos-alvo da genitália externa. A DHT é o andrógeno ativo que induz a virilização:
- O tubérculo genital alonga-se para formar o pênis.
- As pregas uretrais fundem-se na linha média para formar a uretra peniana e parte do corpo do pênis.
- As protuberâncias labioescrotais fundem-se para formar o escroto.
No sexo feminino, na ausência de níveis significativos de andrógenos (particularmente DHT), a genitália externa segue um caminho de desenvolvimento distinto:
- O tubérculo genital desenvolve-se minimamente para formar o clitóris.
- As pregas uretrais permanecem não fundidas e formam os pequenos lábios (lábios menores).
- As protuberâncias labioescrotais também permanecem não fundidas e desenvolvem-se nos grandes lábios (lábios maiores).
Este processo coordenado garante a concordância entre o sexo gonadal, os ductos internos e a genitália externa no desenvolvimento típico.
Impacto da HAC na Diferenciação Sexual
A Hiperplasia Adrenal Congênita (HAC) representa uma causa proeminente de Distúrbios da Diferenciação Sexual (DDS).
Impacto na Diferenciação Sexual Feminina (46,XX)
Em indivíduos com constituição cromossômica 46,XX, a base fisiopatológica reside no bloqueio enzimático na esteroidogênese adrenal, mais comumente envolvendo a 21-hidroxilase. Este defeito impede a síntese adequada de cortisol e aldosterona, levando a um acúmulo de precursores hormonais, como a 17-hidroxiprogesterona (17-OHP). Consequentemente, esses precursores são desviados para a via de síntese androgênica, resultando em produção excessiva de andrógenos, como a testosterona, pelas adrenais fetais.
Durante o desenvolvimento fetal, especificamente entre a 7ª e a 12ª semana de gestação, período crítico para a diferenciação da genitália externa, a exposição do feto geneticamente feminino (46,XX) a níveis suprafisiológicos de andrógenos causa virilização. Clinicamente, isso se manifesta ao nascimento como genitália ambígua.
Manifestações da Virilização Externa
A intensidade da virilização da genitália externa é variável, diretamente correlacionada à severidade da deficiência enzimática e ao grau de exposição androgênica intrauterina. As apresentações clínicas podem abranger um espectro que inclui:
- Clitoromegalia: Hipertrofia do clitóris, variando desde um aumento discreto até uma estrutura que se assemelha a um falo.
- Fusão Labial: União posterior dos lábios maiores, que pode ser parcial ou completa, resultando em uma aparência escrotal.
- Formação de Seio Urogenital: Presença de um canal comum para a uretra e a vagina, com uma única abertura perineal, em contraste com as aberturas distintas normais.
A classificação da gravidade dessas alterações é frequentemente sistematizada pela escala de Prader, que quantifica o grau de ambiguidade genital.
Pseudo-hermafroditismo Feminino e Integridade das Estruturas Internas
A condição em que um indivíduo 46,XX possui gônadas femininas (ovários) e desenvolvimento normal das estruturas derivadas dos ductos de Müller, mas apresenta virilização da genitália externa devido à exposição androgênica pré-natal, é definida como pseudo-hermafroditismo feminino. É fundamental compreender que, na HAC, o excesso de andrógenos adrenais não afeta o desenvolvimento das estruturas müllerianas.
O desenvolvimento do útero, das trompas de Falópio e da porção superior da vagina a partir dos ductos de Müller depende da ausência do Hormônio Anti-Mülleriano (AMH) e não é inibido pela presença de andrógenos. Como a produção de AMH (primariamente testicular) não ocorre em indivíduos 46,XX e os ductos de Wolff regridem na ausência de níveis adequados de testosterona local, as estruturas genitais internas femininas desenvolvem-se normalmente. Portanto, apesar da ambiguidade externa, o útero, as trompas e os ovários são tipicamente normais em pacientes 46,XX com HAC.
Impacto na Diferenciação Sexual Masculina (46,XY) e Desenvolvimento
Em indivíduos geneticamente masculinos (cariótipo 46,XY), a Hiperplasia Adrenal Congênita (HAC) decorrente das deficiências enzimáticas mais comuns, como a de 21-hidroxilase, manifesta-se de forma distinta em comparação aos indivíduos 46,XX. O impacto do excesso androgênico adrenal pode ser menos evidente ao nascimento, mas acarreta consequências significativas no desenvolvimento subsequente.
Ao nascimento, a genitália externa em meninos 46,XY com HAC clássica pode parecer normal ou apresentar apenas alterações sutis. Frequentemente, as manifestações clínicas discretas incluem um leve aumento do tamanho do pênis (macrogenitossomia discreta) e/ou hiperpigmentação da bolsa escrotal. Estas alterações, por vezes, não são imediatamente reconhecidas como patológicas, o que pode atrasar o diagnóstico, especialmente nas formas não perdedoras de sal. É crucial notar que, independentemente da aparência genital, estes indivíduos estão sujeitos ao risco de crise adrenal por perda de sal no período neonatal se houver deficiência concomitante de aldosterona, manifestando-se com hiponatremia, hipercalemia, desidratação e choque.
Consequências do Hiperandrogenismo Persistente
O excesso continuado de andrógenos em meninos 46,XY com HAC não tratada desencadeia uma série de eventos desenvolvimentais precoces. O crescimento peniano pode tornar-se mais acentuado e pode ocorrer pubarca precoce, definida pelo aparecimento de pelos pubianos antes dos 9 anos. Outros sinais de hiperandrogenismo, como acne, também podem surgir prematuramente.
Adicionalmente, o hiperandrogenismo promove uma aceleração da velocidade de crescimento e um avanço da idade óssea em relação à idade cronológica. Embora isso resulte em um crescimento inicial acelerado, o fechamento prematuro das epífises ósseas pode ocorrer, comprometendo a estatura final do indivíduo se o tratamento não for instituído a tempo.
Particularidades da Deficiência de 17α-Hidroxilase
Uma exceção importante ao quadro de excesso androgênico em meninos com HAC é a deficiência de 17α-hidroxilase. Nesta forma específica de HAC, ocorre uma diminuição na produção tanto de cortisol quanto de hormônios sexuais (andrógenos e estrógenos), devido ao bloqueio enzimático afetar ambas as vias. Como consequência, a produção de mineralocorticoides (como a desoxicorticosterona e corticosterona, precursores da aldosterona) pode estar aumentada. Indivíduos 46,XY com esta deficiência enzimática apresentam um quadro de subvirilização ou mesmo diferenciação sexual atípica, manifestando-se com genitália externa feminina ou ambígua ao nascimento, apesar do cariótipo masculino. Frequentemente, associam-se testículos não descendidos (criptorquidia) e hipertensão arterial devido ao excesso de mineralocorticoides.
Portanto, a avaliação do impacto da HAC em indivíduos 46,XY requer atenção tanto às manifestações sutis ao nascimento (aumento peniano, hiperpigmentação escrotal) quanto às consequências desenvolvimentais a longo prazo (puberdade precoce, aceleração do crescimento, comprometimento da estatura final). A identificação de formas mais raras, como a deficiência de 17α-hidroxilase, que paradoxalmente cursam com subvirilização em indivíduos 46,XY, é fundamental para o diagnóstico diferencial dos distúrbios da diferenciação sexual (DDS) e para o manejo clínico adequado.
Manifestações Clínicas Sistêmicas e Tardias
A Hiperplasia Adrenal Congênita (HAC) transcende as alterações na diferenciação sexual e desenvolvimento genital, apresentando um espectro de manifestações clínicas sistêmicas que podem ser agudas e potencialmente fatais no período neonatal (como a crise de perda de sal), além de consequências tardias significativas decorrentes do desequilíbrio hormonal crônico, afetando ambos os sexos.
Crise Adrenal (Perda de Sal) no Período Neonatal
Uma das apresentações mais graves da HAC clássica, especialmente nas primeiras semanas de vida, é a crise adrenal ou crise de perda de sal. Esta emergência médica resulta primariamente da deficiência combinada de cortisol e aldosterona, hormônios essenciais para a manutenção da homeostase.
A deficiência de aldosterona compromete gravemente o equilíbrio hidroeletrolítico. A incapacidade dos túbulos renais distais em reabsorver sódio adequadamente leva à sua perda excessiva na urina, resultando em hiponatremia e consequente desidratação e hipovolemia. Simultaneamente, a excreção de potássio é diminuída, causando hipercalemia, uma condição que acarreta risco significativo de arritmias cardíacas e outras complicações graves. A deficiência de cortisol agrava o quadro, contribuindo para a hipotensão, diminuição da resposta fisiológica ao estresse e, frequentemente, hipoglicemia.
Clinicamente, a crise de perda de sal manifesta-se em recém-nascidos com sintomas inespecíficos como vômitos, dificuldade de ganho de peso, letargia e desidratação progressiva, que podem evoluir rapidamente para choque hipovolêmico. A identificação precoce dos distúrbios eletrolíticos (hiponatremia, hipercalemia) e da hipoglicemia, juntamente com os sinais clínicos, é crucial para o diagnóstico e intervenção imediatos.
Manifestações Tardias e Decorrentes do Hiperandrogenismo
O bloqueio enzimático na via de síntese de cortisol e aldosterona desvia os precursores para a produção excessiva de andrógenos adrenais. Este hiperandrogenismo crônico é a base para diversas manifestações clínicas que podem surgir mais tardiamente na infância, adolescência ou vida adulta, sendo características tanto da forma não clássica (HANC) quanto da forma clássica inadequadamente tratada.
- Pubarca Precoce: Define-se pelo aparecimento prematuro de pelos pubianos (antes dos 8 anos em meninas e 9 anos em meninos). Este é frequentemente um dos primeiros sinais de excesso androgênico pós-natal, podendo vir acompanhado de acne e odor axilar. A avaliação deve incluir a velocidade de crescimento e a maturação óssea.
- Sinais de Hiperandrogenismo Cutâneo: Em adolescentes e adultos, especialmente mulheres, manifestações como hirsutismo (crescimento excessivo de pelos em padrão masculino), acne persistente ou severa e, por vezes, alopecia androgenética são comuns.
- Irregularidades Menstruais e Infertilidade: Em mulheres, o ambiente hiperandrogênico pode interferir na esteroidogênese ovariana e na dinâmica hipotálamo-hipófise-ovariana, levando à disfunção ovulatória crônica. Isto se manifesta clinicamente como oligomenorreia (ciclos menstruais infrequentes) ou amenorreia (ausência de menstruação). A infertilidade pode ser uma consequência tanto em mulheres quanto em homens com HAC não controlada.
- Alterações no Crescimento e Estatura Final: A exposição precoce e/ou excessiva a andrógenos estimula a maturação esquelética. Clinicamente, isso se traduz em um avanço da idade óssea em relação à idade cronológica e um crescimento linear inicialmente acelerado durante a infância. Contudo, este avanço na maturação óssea leva a um fechamento prematuro das epífises dos ossos longos, comprometendo o potencial de crescimento estatural e resultando, frequentemente, em uma baixa estatura na vida adulta.
Estas manifestações sistêmicas e tardias ressaltam a natureza complexa da HAC e a necessidade de um acompanhamento endocrinológico contínuo para otimizar o tratamento hormonal substitutivo, monitorar o controle androgênico e mitigar os efeitos deletérios sobre o desenvolvimento puberal, a função reprodutiva, o metabolismo e o crescimento.
Diagnóstico e Formas da HAC
Avaliação Inicial e Diagnóstico
Diante de um neonato com genitália ambígua, a abordagem diagnóstica inicial é crucial. A investigação deve incluir uma anamnese detalhada, abrangendo histórico familiar de consanguinidade, óbitos neonatais inexplicados ou outros casos de genitália atípica. Exames fundamentais incluem a determinação do cariótipo e a dosagem de 17-hidroxiprogesterona (17-OHP). O cariótipo é essencial para identificar a constituição cromossômica (46,XX ou 46,XY) e auxiliar na exclusão de outras condições genéticas, sendo a concordância entre o cariótipo e a genitália interna um fator importante na definição etiológica. Níveis elevados de 17-OHP, particularmente no contexto de genitália ambígua, sugerem fortemente a Hiperplasia Adrenal Congênita (HAC) por deficiência de 21-hidroxilase. Exames complementares podem ser necessários para confirmar o diagnóstico e diferenciar de outras causas de distúrbios da diferenciação sexual.
HAC e os Distúrbios da Diferenciação Sexual (DDS)
Os Distúrbios da Diferenciação Sexual (DDS) compreendem condições congênitas com desenvolvimento atípico do sexo cromossômico, gonadal ou anatômico (genitália interna e/ou externa). A HAC representa uma causa importante de DDS, particularmente em indivíduos com cariótipo 46,XX. Nesses casos, a exposição fetal a níveis elevados de andrógenos adrenais, resultante da deficiência enzimática (principalmente 21-hidroxilase), causa virilização da genitália externa durante o período entre a 7ª e a 12ª semana de gestação. Esta condição, onde indivíduos 46,XX possuem genitália interna feminina normal (útero, trompas, ovários) mas apresentam virilização externa de graus variáveis, é conhecida como pseudo-hermafroditismo feminino. A intensidade da virilização depende da gravidade da deficiência enzimática.
Formas Clínicas da HAC
As manifestações clínicas da HAC variam conforme a gravidade da deficiência enzimática, distinguindo-se principalmente as formas clássica e não clássica.
Forma Clássica
A forma clássica é a mais grave e subdivide-se em perdedora de sal e virilizante simples, ambas resultantes de deficiência severa de 21-hidroxilase.
- Perdedora de Sal: Caracteriza-se pela deficiência acentuada de cortisol e aldosterona. Manifesta-se tipicamente no período neonatal, nas primeiras semanas de vida, com crise adrenal ou crise de perda de sal. Os sintomas incluem vômitos, desidratação, dificuldade de ganho de peso, hipoglicemia, hipotensão, hiponatremia e hipercalemia, podendo evoluir para choque hipovolêmico. Em meninas (46,XX), a exposição intrauterina ao excesso de andrógenos causa virilização da genitália externa, resultando em genitália ambígua ao nascimento (graus variáveis de clitoromegalia, fusão labial, podendo formar um seio urogenital comum). Em meninos (46,XY), a genitália pode parecer normal ao nascimento ou apresentar sinais sutis como aumento peniano ou hiperpigmentação escrotal, estando igualmente sujeitos à crise de perda de sal.
- Virilizante Simples: Nesta forma, há deficiência de cortisol suficiente para causar hiperplasia adrenal e excesso de andrógenos, mas a produção de aldosterona é relativamente preservada, evitando a crise de perda de sal neonatal. A principal manifestação em meninas (46,XX) é a genitália ambígua ao nascimento devido à virilização pré-natal, com graus variáveis (desde clitoromegalia até fusão labial completa). Em meninos (46,XY), os sinais ao nascimento podem ser ausentes ou discretos (aumento peniano, hiperpigmentação escrotal). Se não tratados, ambos os sexos podem apresentar sinais de hiperandrogenismo mais tarde, como pubarca precoce e avanço da idade óssea com consequente aceleração do crescimento e potencial baixa estatura final.
Forma Não Clássica (HANC ou Tardia)
A forma não clássica (HANC) resulta de uma deficiência enzimática mais branda e manifesta-se mais tardiamente, na infância, adolescência ou vida adulta. Os pacientes não apresentam genitália ambígua ao nascimento nem crises de perda de sal. As manifestações clínicas decorrem do hiperandrogenismo leve a moderado e podem incluir pubarca precoce (aparecimento de pelos pubianos antes dos 8 anos em meninas e 9 anos em meninos), aceleração da velocidade de crescimento e avanço da maturação óssea, acne, hirsutismo, irregularidades menstruais (oligomenorreia ou amenorreia), e infertilidade. Em mulheres, o quadro pode mimetizar a Síndrome dos Ovários Policísticos (SOP). Em homens, pode levar a puberdade precoce ou infertilidade.
Outras Formas (Deficiência de 17α-hidroxilase)
Embora a deficiência de 21-hidroxilase seja a causa mais comum de HAC, outras deficiências enzimáticas devem ser consideradas. A deficiência de 17α-hidroxilase, por exemplo, cursa com diminuição da produção de cortisol e de hormônios sexuais (andrógenos e estrógenos), mas com acúmulo de precursores com atividade mineralocorticoide, levando ao aumento da reabsorção de sódio e hipertensão. Clinicamente, indivíduos geneticamente femininos (46,XX) apresentam ausência de desenvolvimento de características sexuais secundárias (infantilismo sexual) e hipertensão. Indivíduos geneticamente masculinos (46,XY) manifestam-se com genitália externa feminina ou ambígua (pseudo-hermafroditismo masculino), testículos não descendidos e hipertensão.
Conclusão
A Hiperplasia Adrenal Congênita (HAC) é uma condição complexa que exige atenção multidisciplinar desde o período neonatal até a vida adulta. Suas implicações no desenvolvimento sexual, equilíbrio hormonal e homeostase metabólica ressaltam a importância do diagnóstico precoce, tratamento adequado e acompanhamento contínuo. O conhecimento detalhado das diferentes formas clínicas, manifestações sistêmicas e particularidades de cada caso é fundamental para garantir a qualidade de vida e o bem-estar dos pacientes afetados por esta condição.