As Doenças Inflamatórias Intestinais (DII), como a Doença de Crohn (DC) e a Retocolite Ulcerativa (RCU), representam um desafio complexo na área da saúde devido à sua etiopatogenia multifatorial. Este artigo oferece uma análise detalhada dos fatores genéticos, imunológicos, ambientais e de risco associados a essas condições inflamatórias crônicas do trato gastrointestinal, visando fornecer uma compreensão abrangente de sua origem e desenvolvimento.
Visão Geral da Etiopatogenia Multifatorial das DII
As Doenças Inflamatórias Intestinais (DII) englobam patologias como a Doença de Crohn (DC) e a Retocolite Ulcerativa (RCU), caracterizadas como distúrbios inflamatórios crônicos do trato gastrointestinal. Sua etiopatogenia é reconhecidamente complexa e multifatorial, não sendo atribuível a uma única causa, mas sim a uma interação dinâmica entre múltiplos fatores.
A base fisiopatológica das DII reside na interação entre uma predisposição genética do indivíduo, disfunções inerentes ao sistema imunológico (particularmente o associado à mucosa intestinal), alterações na composição e função da microbiota intestinal (disbiose) e a exposição a diversos fatores ambientais. Nenhum desses elementos, isoladamente, é suficiente para causar a doença.
O paradigma central na etiopatogenia das DII postula que, em indivíduos geneticamente suscetíveis, ocorre uma resposta imunológica desregulada, inadequada e exacerbada contra antígenos presentes no lúmen intestinal, primariamente componentes da microbiota comensal. Esta perda de tolerância imunológica desencadeia e perpetua um processo inflamatório crônico na parede intestinal.
A influência genética é inegável, suportada por estudos de concordância em gêmeos monozigóticos ser superior àquela em dizigóticos, e pela observação de agregação familiar. Contudo, a concordância incompleta mesmo em gêmeos idênticos demonstra cabalmente que fatores não genéticos, majoritariamente ambientais, são indispensáveis para a manifestação clínica da doença. Fatores ambientais, incluindo dieta, tabagismo (com efeitos paradoxais entre DC e RCU), infecções prévias e uso de certos medicamentos, modulam o risco em indivíduos predispostos, possivelmente ao influenciar a microbiota ou diretamente a resposta imune e a integridade da barreira intestinal.
Em suma, a etiopatogenia das DII representa um modelo de doença complexa onde a suscetibilidade genética interage com gatilhos e moduladores ambientais, culminando em uma resposta imune aberrante à microbiota intestinal, que se traduz clinicamente como inflamação intestinal crônica.
Predisposição Genética e Influência Familiar nas DII
A etiopatogenia das Doenças Inflamatórias Intestinais (DII), compreendendo a Doença de Crohn (DC) e a Retocolite Ulcerativa (RCU), é reconhecida como multifatorial. Dentre os fatores envolvidos, a predisposição genética assume um papel significativo na suscetibilidade individual ao desenvolvimento destas condições crônicas. Embora não sejam consideradas doenças estritamente hereditárias, pois a maioria dos casos é esporádica, a influência genética é inegável.
Evidências da Influência Genética e Agregação Familiar
A relevância do componente genético é fortemente sugerida por estudos de concordância em gêmeos, que demonstram taxas significativamente maiores de DII em gêmeos monozigóticos (idênticos) em comparação com gêmeos dizigóticos (fraternos). Adicionalmente, observa-se uma agregação familiar, sendo a história familiar positiva um fator de risco importante. Indivíduos com parentes de primeiro grau afetados por DII apresentam um risco aumentado de desenvolver a doença, com relatos indicando que cerca de 5 a 10% dos pacientes possuem outros familiares acometidos. Contudo, a concordância em gêmeos monozigóticos não atinge 100%, e a maioria dos pacientes não possui histórico familiar, evidenciando a importância de outros fatores e o conceito de penetrância incompleta. Isso significa que a presença de genes de suscetibilidade aumenta o risco, mas não garante o desenvolvimento da doença, sendo necessária a interação com fatores ambientais.
Genes de Suscetibilidade Identificados
Pesquisas genômicas, incluindo Estudos de Associação Genômica Ampla (GWAS), identificaram múltiplos genes e loci associados a um risco aumentado de desenvolver DII. Esses genes frequentemente estão envolvidos em vias essenciais para a manutenção da homeostase intestinal, tais como:
- Regulação da Resposta Imune: Múltiplos genes implicados modulam tanto a imunidade inata quanto a adaptativa, influenciando a interação do sistema imune com a microbiota intestinal.
- Função da Barreira Epitelial Intestinal: Genes relacionados à integridade estrutural e funcional da barreira mucosa, cuja disfunção é um elemento chave na patogênese das DII.
- Autofagia: Genes que regulam o processo de autofagia, essencial para o manejo de componentes celulares e patógenos intracelulares, podem ter seu funcionamento alterado.
Dentre as associações genéticas mais robustas encontra-se a relacionada ao gene NOD2/CARD15 (Nucleotide-binding oligomerization domain-containing protein 2 / Caspase recruitment domain-containing protein 15). Polimorfismos neste gene, que codifica um receptor intracelular da imunidade inata reconhecedor de peptidoglicano bacteriano, estão fortemente associados a um aumento na suscetibilidade à Doença de Crohn, particularmente em populações caucasianas. Variantes neste gene podem resultar em uma resposta imune alterada frente à microbiota intestinal, contribuindo para o processo inflamatório crônico característico da DC.
Em suma, a predisposição genética é um componente fundamental na etiopatogenia das DII, interagindo com fatores imunológicos e ambientais de maneira complexa para determinar o risco individual e a potencial manifestação da doença.
Disfunção Imunológica e Resposta Inflamatória Crônica
A disfunção do sistema imunológico é um pilar fundamental na etiopatogenia multifatorial das Doenças Inflamatórias Intestinais (DII), abrangendo tanto a Doença de Crohn (DC) quanto a Retocolite Ulcerativa (RCU). Evidências apontam que uma resposta imunológica exacerbada, inadequada e desregulada contra componentes da microbiota intestinal e antígenos luminais, ocorrendo em indivíduos geneticamente predispostos, desempenha um papel central no desencadeamento e perpetuação dessas condições.
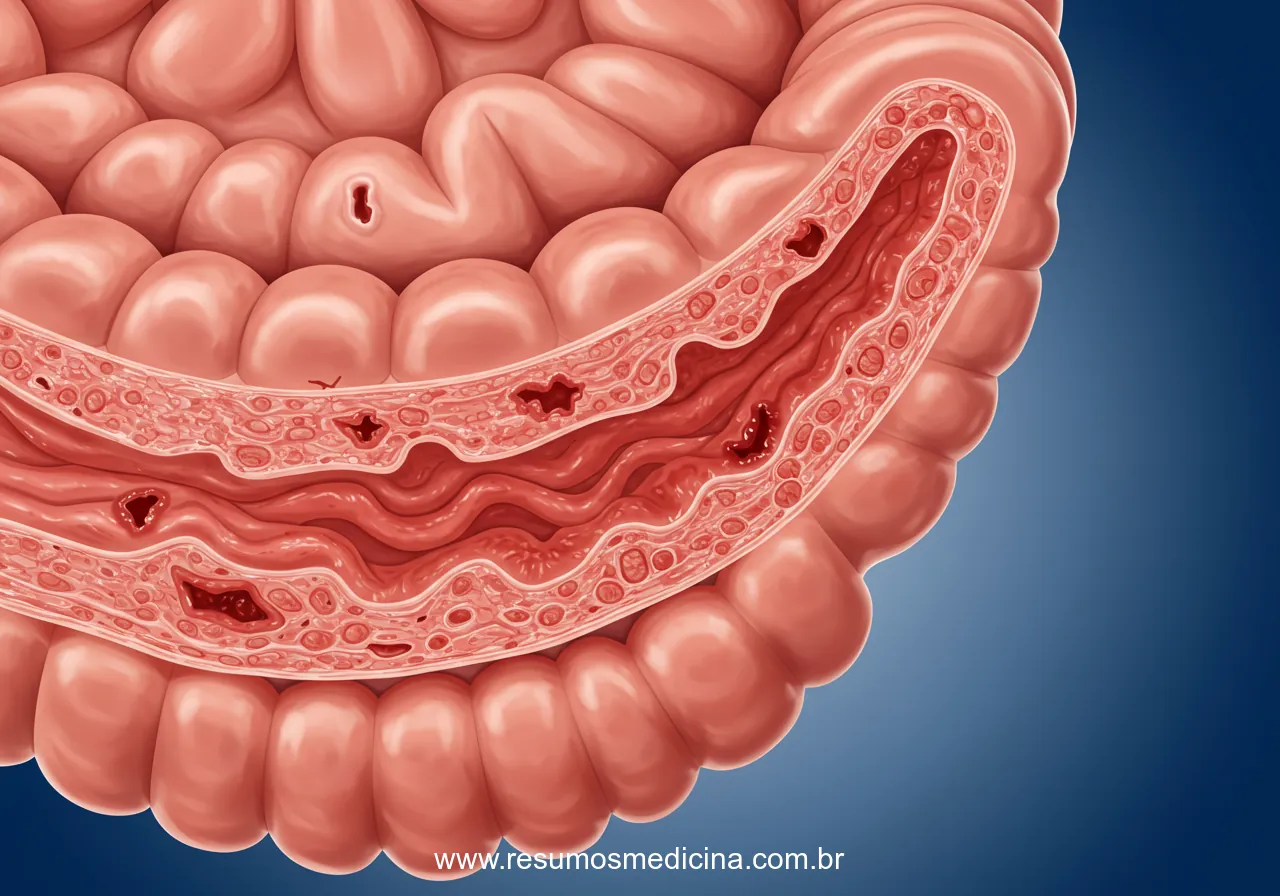
Esta resposta imune anômala manifesta-se como uma inflamação crônica na mucosa intestinal. Na RCU, essa inflamação é tipicamente restrita à mucosa e submucosa do cólon e reto. Em contraste, na DC, a inflamação é caracteristicamente transmural, afetando todas as camadas da parede intestinal e podendo ocorrer em qualquer segmento do trato gastrointestinal. Independentemente da localização e profundidade, essa inflamação persistente é a força motriz por trás do dano tecidual observado nas DII.
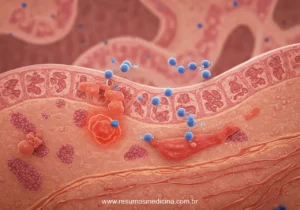
A manutenção deste estado inflamatório crônico envolve mecanismos celulares e moleculares complexos. Observa-se uma significativa infiltração da parede intestinal por células inflamatórias, incluindo um papel fundamental das células T na perpetuação da resposta imune, particularmente na RCU. Essas células, juntamente com outras do sistema imune, liberam um arsenal de mediadores inflamatórios.
Entre os mediadores cruciais estão as citocinas pró-inflamatórias. Estudos sobre a fisiopatologia da RCU e outras condições inflamatórias associadas, como a colite fulminante e a anemia de doença crônica, destacam o papel de citocinas como o Fator de Necrose Tumoral alfa (TNF-alfa), Interleucina-1 (IL-1) e Interleucina-6 (IL-6). Estas moléculas amplificam e sustentam a cascata inflamatória, contribuindo diretamente para o dano tecidual.
A consequência direta desta resposta imune desregulada e da inflamação crônica mediada por citocinas é o dano tecidual progressivo. Manifestações como ulcerações na mucosa, sangramento, e, em casos mais graves, como na colite fulminante, potencial necrose da parede colônica, são resultantes diretos da atividade inflamatória descontrolada. Portanto, a disfunção imunológica, caracterizada por uma resposta inadequada a estímulos intraluminais, é o evento chave que culmina na inflamação crônica e nas lesões teciduais definidoras das DII.
Fatores Ambientais: Gatilhos e Moduladores de Risco
A etiopatogenia das Doenças Inflamatórias Intestinais (DII) é reconhecidamente multifatorial, envolvendo uma complexa interação entre predisposição genética, disfunção do sistema imune da mucosa e diversos fatores ambientais. Estes últimos atuam como potenciais gatilhos ou moduladores do risco em indivíduos geneticamente suscetíveis, influenciando o desenvolvimento e a progressão da Doença de Crohn (DC) e da Retocolite Ulcerativa (RCU). A constatação de que a concordância para DII não atinge 100% mesmo em gêmeos monozigóticos ressalta a importância crucial desses fatores exógenos no desenvolvimento da doença.
Principais Fatores Ambientais Identificados
Diversos elementos ambientais foram associados ao risco de DII, atuando frequentemente sobre a microbiota intestinal e a resposta imune do hospedeiro. Com base nas fontes disponíveis, destacam-se:
- Dieta: Fatores dietéticos são consistentemente citados como influências ambientais relevantes na etiopatogenia das DII. Embora os componentes específicos da dieta não sejam detalhados nos conteúdos fornecidos, sua importância como fator ambiental modulador é reconhecida.
- Uso de Anti-inflamatórios não Esteroidais (AINEs): O uso de AINEs é identificado como um fator de risco ambiental associado às DII, podendo influenciar seu desenvolvimento ou exacerbação.
- Infecções Gastrointestinais: Evidências sugerem que infecções gastrointestinais, particularmente aquelas ocorridas em fases precoces da vida, estão associadas a um risco aumentado de desenvolver DII. Acredita-se que a disbiose intestinal resultante de infecções (ou outros fatores) possa desencadear ou exacerbar a resposta inflamatória desregulada característica das DII.
- Uso de Antibióticos: O emprego de antibióticos é considerado um fator de risco ambiental. Seu impacto potencial na composição da microbiota intestinal pode contribuir para a disbiose frequentemente observada em pacientes com DII.
- Higiene: Fatores relacionados à higiene são mencionados como potenciais influências ambientais no desenvolvimento das DII, embora os mecanismos específicos não sejam detalhados no material fornecido.
- Microbiota Intestinal: Alterações na microbiota intestinal (disbiose) são um elo crucial entre fatores ambientais e a resposta imune. Fatores como dieta, infecções e antibióticos modulam a microbiota, que por sua vez interage com o sistema imune, contribuindo para a resposta desregulada vista nas DII.
Fatores Moduladores Específicos
Além dos fatores de risco gerais, alguns elementos ambientais apresentam efeitos moduladores mais específicos:
- Apendicectomia Prévia: Estudos epidemiológicos indicam que a realização prévia de apendicectomia está associada a um risco reduzido de desenvolvimento subsequente da Retocolite Ulcerativa (RCU).
Menção ao Tabagismo
O tabagismo constitui um fator ambiental chave, cujo impacto nas DII é notavelmente distinto entre a DC e a RCU. É um fator de risco bem estabelecido para o desenvolvimento e curso mais agressivo da Doença de Crohn, enquanto, paradoxalmente, parece exercer um efeito protetor contra a Retocolite Ulcerativa. Devido à sua relevância e complexidade, a influência do tabagismo será detalhada em seção própria neste artigo.
Em síntese, a compreensão dos fatores ambientais e sua interação com a predisposição genética e a resposta imune é fundamental para desvendar a etiopatogenia das DII. A exposição a esses elementos em indivíduos geneticamente suscetíveis pode perturbar a homeostase intestinal e desencadear a cascata inflamatória crônica que define estas doenças.
Tabagismo: Impacto Diferencial e Paradoxal nas DII
O tabagismo representa um fator ambiental de grande relevância na etiopatogenia das Doenças Inflamatórias Intestinais (DII), exercendo influências notavelmente distintas e opostas na Doença de Crohn (DC) e na Retocolite Ulcerativa (RCU). Este impacto diferencial é um aspecto crucial na compreensão dos fatores de risco e na evolução clínica destas condições.
Impacto na Doença de Crohn (DC)
Na Doença de Crohn, o tabagismo é um fator de risco bem estabelecido, associado a um aumento da incidência e gravidade da doença. A sua influência negativa manifesta-se em múltiplos aspectos do curso clínico:
- Aumento do Risco e Agressividade: Fumar está associado a um risco aumentado de desenvolver DC e a um curso clínico mais agressivo da doença.
- Maior Necessidade de Intervenções: Pacientes tabagistas com DC apresentam maior necessidade de cirurgias e de terapia com imunossupressores.
- Redução da Resposta Terapêutica: O tabagismo demonstrou reduzir a resposta à terapia medicamentosa.
- Risco de Complicações: É um fator de risco conhecido para o desenvolvimento e a recorrência de fístulas perianais, uma complicação significativa da DC.
De forma relevante para a prática clínica, a cessação do tabagismo em pacientes com Doença de Crohn está associada a um melhor prognóstico.
Impacto Paradoxal na Retocolite Ulcerativa (RCU)
Em contraste marcante com a DC, o tabagismo demonstra um efeito paradoxalmente protetor em relação à Retocolite Ulcerativa. Estudos epidemiológicos indicam que:
- Menor Risco em Fumantes Ativos: O tabagismo corrente está associado a um menor risco de desenvolvimento de RCU. Não fumantes e ex-fumantes apresentam maior risco em comparação com fumantes ativos.
- Possível Curso Clínico Mais Leve: Há sugestões de que o tabagismo possa estar associado a um curso clínico menos agressivo da RCU.
- Risco Associado à Cessação: A suspensão do tabagismo pode precipitar o aparecimento da RCU em alguns indivíduos ou levar à exacerbação dos sintomas em pacientes já diagnosticados.
- Efeito do Tabagismo Prévio: Embora o tabagismo corrente confira proteção, existem indicações de que o tabagismo prévio possa, paradoxalmente, aumentar o risco de desenvolver RCU.
É crucial enfatizar que, apesar deste efeito protetor específico para a RCU, os múltiplos e graves malefícios do tabagismo à saúde geral superam qualquer potencial benefício localizado, não sendo recomendado como estratégia terapêutica ou preventiva.
Mecanismos Subjacentes e Considerações Adicionais
Os mecanismos exatos subjacentes a estes efeitos opostos do tabagismo nas DII não são totalmente compreendidos. As hipóteses atuais sugerem que o tabagismo pode modular a resposta imune da mucosa intestinal, alterar a composição e função da microbiota intestinal e influenciar a permeabilidade da barreira intestinal de formas distintas na DC e na RCU. Adicionalmente, exposições ambientais como o tabagismo podem também modular a expressão de biomarcadores sorológicos, como ASCA e p-ANCA, associados às DII.
Entendendo a Fisiopatologia da Retocolite Ulcerativa (RCU)
A Retocolite Ulcerativa (RCU) é uma doença inflamatória intestinal crônica caracterizada por um processo inflamatório que acomete primariamente a mucosa e a submucosa do cólon e do reto. Sua etiopatogenia é considerada multifatorial, resultante da interação entre uma predisposição genética, disfunção do sistema imunológico, alterações na microbiota intestinal e fatores ambientais.
O cerne da fisiopatologia da RCU reside em uma resposta imune desregulada e exacerbada contra antígenos luminais, particularmente componentes da microbiota intestinal, em indivíduos geneticamente suscetíveis. Estudos apontam para um papel fundamental das células T na perpetuação da inflamação, através da produção de diversas citocinas pró-inflamatórias, como o fator de necrose tumoral alfa (TNF-α), interleucina-1 (IL-1) e interleucina-6 (IL-6). Essa resposta imune inadequada é responsável pelo dano tecidual observado na doença.
A inflamação na RCU possui características distintivas. Ela é tipicamente limitada às camadas mais superficiais da parede intestinal (mucosa e submucosa) e apresenta um padrão de distribuição contínuo. O processo inflamatório geralmente se inicia no reto e se estende de forma proximal e ascendente ao longo do cólon, podendo acometer desde apenas o reto (proctite) até todo o cólon (pancolite).
Como resultado direto da inflamação crônica, ocorre dano à barreira epitelial intestinal e à estrutura da mucosa, levando à formação de ulcerações e consequente sangramento. Estas alterações anatomopatológicas são a base para os sintomas característicos da RCU, como diarreia sanguinolenta, dor abdominal e urgência retal.
É crucial diferenciar a fisiopatologia da RCU da Doença de Crohn (DC). Ao contrário da RCU, a DC pode afetar qualquer parte do trato gastrointestinal (da boca ao ânus) e a inflamação é tipicamente transmural, ou seja, acomete todas as camadas da parede intestinal. Além disso, a inflamação na DC frequentemente apresenta um padrão descontínuo ou segmentar (“lesões salteadas”). Essas diferenças fisiopatológicas explicam as distintas manifestações clínicas e complicações associadas a cada uma dessas doenças inflamatórias intestinais.
Entendendo a Fisiopatologia da Doença de Crohn (DC)
A Doença de Crohn (DC) é uma condição inflamatória intestinal crônica cuja fisiopatologia é reconhecidamente complexa e multifatorial. A sua etiologia, embora não completamente elucidada, envolve uma intrincada interação entre predisposição genética, fatores ambientais, disfunção do sistema imunológico e alterações na microbiota intestinal. Acredita-se que uma resposta imune exacerbada e desregulada contra componentes da microbiota intestinal, em indivíduos geneticamente susceptíveis, constitui o evento central que desencadeia e perpetua o processo inflamatório crônico.
Um aspecto distintivo da DC é a sua capacidade de acometer qualquer segmento do trato gastrointestinal, desde a boca até o ânus. No entanto, observa-se uma predileção pelo íleo terminal e pelo cólon como os sítios mais frequentemente afetados. A característica patológica fundamental da DC é a natureza transmural da inflamação, ou seja, o processo inflamatório compromete todas as camadas da parede intestinal, desde a mucosa até a serosa.
Essa inflamação transmural é a base para o desenvolvimento das complicações típicas da doença. A lesão profunda da parede intestinal predispõe à formação de:
- Estenoses: Áreas de estreitamento do lúmen intestinal resultantes da fibrose cicatricial secundária à inflamação crônica.
- Fístulas: Trajetos anormais que conectam o intestino a outras estruturas, como outros segmentos intestinais, pele (enterocutâneas), bexiga (enterovesicais) ou vagina (enterovaginais). As manifestações perianais, como fístulas, fissuras e abscessos perianais, são particularmente comuns na DC, afetando uma parcela significativa dos pacientes, e derivam diretamente dessa característica inflamatória transmural na região.
- Abscessos: Coleções purulentas que podem se formar na parede intestinal ou na cavidade abdominal como resultado da penetração bacteriana através da parede intestinal comprometida.
A etiopatogenia reforça a importância da interação de múltiplos fatores. A disfunção da barreira intestinal, que permite maior contato entre antígenos luminais (microbiota) e o sistema imune da mucosa, é um componente crucial. Fatores genéticos desempenham um papel significativo, com destaque para polimorfismos no gene NOD2/CARD15, que está fortemente associado à suscetibilidade à DC, especialmente em populações caucasianas. Este gene codifica um receptor intracelular da imunidade inata que reconhece componentes bacterianos, e suas variantes alteram a resposta imune à microbiota. Assim, a fisiopatologia da DC resulta de uma complexa cascata de eventos iniciada por fatores genéticos e ambientais, levando à disfunção da barreira, resposta imune desregulada à microbiota e inflamação transmural crônica com suas consequentes complicações.
Fatores de Risco Adicionais, Epidemiologia e Curso da Doença
A compreensão dos fatores de risco adicionais, dos padrões epidemiológicos e dos preditores de curso da doença é fundamental na abordagem clínica das Doenças Inflamatórias Intestinais (DII).
Epidemiologia e Fatores de Risco
As DII, incluindo a Doença de Crohn (DC) e a Retocolite Ulcerativa (RCU), exibem padrões epidemiológicos específicos. A RCU, em particular, apresenta uma distribuição bimodal de incidência, com picos entre os 15 e os 30 anos e, posteriormente, entre os 50 e os 70 anos. Embora o pico de incidência das DII ocorra entre 15 e 30 anos, é relevante notar que 20-30% dos casos manifestam-se antes dos 18 anos, podendo surgir inclusive na infância.
Além dos fatores genéticos, imunológicos e da microbiota, outros elementos ambientais e individuais influenciam o risco de desenvolver DII:
- Tabagismo: Exerce efeitos distintos e opostos. É um fator de risco conhecido para a DC, associado a um curso mais agressivo, maior necessidade de cirurgia e recorrência pós-operatória. Paradoxalmente, o tabagismo corrente demonstra um efeito protetor contra o desenvolvimento da RCU, com não fumantes e ex-fumantes apresentando maior risco. A cessação do tabagismo, no entanto, pode precipitar ou exacerbar a RCU em alguns pacientes. Apesar deste efeito protetor na RCU, os malefícios gerais do tabagismo contraindicam seu uso.
- Apendicectomia: Estudos têm associado a apendicectomia prévia a um risco reduzido de desenvolver RCU.
- Outros Fatores Ambientais: O uso de anti-inflamatórios não esteroidais (AINEs), fatores dietéticos, infecções gastrointestinais (especialmente em fases precoces da vida), uso de antibióticos e, em algumas populações, o uso de contraceptivos orais (associado a um discreto aumento no risco) são citados como fatores ambientais que podem modular o risco de DII.
Preditores do Curso da Doença
Certos fatores clínicos e demográficos podem indicar um curso mais agressivo da doença, alertando para a necessidade de estratégias terapêuticas mais intensivas:
- Retocolite Ulcerativa (RCU): Fatores associados a um curso mais agressivo incluem o diagnóstico em idade jovem (inferior a 40 anos), a extensão da doença (pancolite), a necessidade prévia de corticoterapia e hospitalizações frequentes devido a exacerbações.
- Doença de Crohn (DC): As fístulas perianais são complicações frequentes, e fatores de risco para seu desenvolvimento e recorrência incluem o tabagismo e a idade jovem ao diagnóstico.
A identificação precoce desses fatores de risco e preditores de curso da doença permite um manejo mais direcionado e potencialmente melhora os desfechos clínicos para os pacientes com DII.
Complicações Sistêmicas Ligadas à Etiopatogenia das DII
A etiopatogenia multifatorial das Doenças Inflamatórias Intestinais (DII), envolvendo uma resposta imune desregulada, inflamação crônica e disfunção da barreira intestinal, não se restringe ao trato gastrointestinal. Diversas complicações sistêmicas importantes derivam diretamente desses mecanismos fisiopatológicos subjacentes.
Anemia nas DII
A anemia é uma complicação frequente, decorrente de múltiplos fatores intrinsecamente ligados à patogênese das DII:
- Anemia Ferropriva: Comum, especialmente em quadros de inflamação ativa e sangramento gastrointestinal. A perda crônica de sangue devido a ulcerações na mucosa (particularmente na Retocolite Ulcerativa – RCU) e diarreia sanguinolenta leva à depleção de ferro. Adicionalmente, a inflamação crônica e a má absorção (mais relevante na Doença de Crohn – DC – ileal) podem comprometer a absorção de ferro, contribuindo para a deficiência. Caracteriza-se por anemia microcítica.
- Anemia de Doença Crônica (ADC) / Anemia Inflamatória: Resulta diretamente da inflamação sistêmica crônica. Citocinas pró-inflamatórias (como a Interleucina-6) afetam a eritropoiese e o metabolismo do ferro. Ocorre um aumento na produção hepática de hepcidina, hormônio que regula o metabolismo do ferro. A hepcidina liga-se à ferroportina (principal exportador de ferro celular), induzindo sua internalização e degradação. Isso resulta na retenção de ferro nos macrófagos e enterócitos, diminuindo a disponibilidade de ferro para a formação de hemoglobina, apesar de estoques corporais potencialmente adequados. Laboratorialmente, cursa com ferro sérico e saturação de transferrina diminuídos, mas ferritina normal ou aumentada. Caracteriza-se por anemia normocítica.
Outros tipos, como anemia macrocítica por deficiência de vitamina B12 ou folato (devido à má absorção, especialmente na DC ileal) ou induzida por medicamentos (ex: sulfasalazina), também podem ocorrer.
Hipoalbuminemia
A baixa concentração de albumina sérica (hipoalbuminemia) é outra manifestação sistêmica comum nas DII. Sua patogênese envolve:
- Enteropatia Perdedora de Proteínas: A inflamação da mucosa intestinal aumenta a permeabilidade, levando à perda de albumina e outras proteínas para o lúmen intestinal.
- Inflamação Sistêmica: O estado inflamatório crônico pode diminuir a síntese hepática de albumina e aumentar seu catabolismo.
Clinicamente, a hipoalbuminemia pode contribuir para a formação de edema, dificuldades na cicatrização e maior susceptibilidade a infecções.
Distúrbios Ósseo-Metabólicos: Osteopenia e Osteoporose
Pacientes com DII, incluindo crianças e adolescentes, apresentam risco aumentado de desenvolver osteopenia (redução da densidade mineral óssea) e osteoporose (redução da massa óssea). Os fatores de risco estão ligados à doença e seu tratamento:
- Inflamação Crônica Sistêmica: Citocinas inflamatórias podem afetar diretamente o metabolismo ósseo.
- Má Absorção: A inflamação intestinal pode levar à má absorção de cálcio e vitamina D, essenciais para a saúde óssea.
- Uso de Corticosteroides: Terapia comum nas DII, os corticosteroides têm efeitos deletérios conhecidos sobre a massa óssea.
- Inatividade Física: Pode ser uma consequência da sintomatologia da doença.
A prevenção foca no controle da inflamação da DII, suplementação adequada de cálcio e vitamina D, estímulo à atividade física e, quando necessário, terapias específicas anti-osteoporose.
Risco Aumentado de Carcinoma Colorretal (CCR)
A inflamação crônica persistente na mucosa colônica, característica tanto da RCU quanto da DC com envolvimento colônico, é um fator de risco estabelecido para o desenvolvimento de displasia e carcinoma colorretal. O risco aumenta significativamente com:
- Duração da Doença: Particularmente em pacientes com diagnóstico há muitos anos.
- Extensão da Inflamação: O risco é maior em casos de acometimento extenso do cólon (ex: pancolite na RCU).
- Gravidade da Inflamação: Inflamação persistente e de difícil controle eleva o risco.
Devido a esse risco aumentado, a vigilância endoscópica regular com biópsias seriadas é fundamental para a detecção precoce de lesões pré-malignas (displasia) ou malignas em pacientes com DII de longa data e/ou extenso acometimento colônico.
Conclusão
Em resumo, a etiopatogenia das DII é intrincada, envolvendo a interação de predisposição genética, disfunção imunológica, alterações na microbiota intestinal e fatores ambientais. A compreensão detalhada desses elementos é crucial para o desenvolvimento de estratégias terapêuticas mais eficazes e para a identificação de medidas preventivas que possam reduzir o impacto dessas doenças na saúde dos indivíduos. A influência do tabagismo, com seus efeitos paradoxais, e as diversas complicações sistêmicas ressaltam a natureza multifacetada das DII, exigindo uma abordagem clínica abrangente e personalizada.