O Carcinoma Ductal In Situ (CDIS) é uma neoplasia maligna não invasiva da mama, originada da proliferação de células epiteliais anormais que revestem os ductos mamários. Classificado como uma lesão precursora do carcinoma ductal invasivo, o CDIS apresenta variações significativas. Este artigo aborda a classificação histológica e molecular do CDIS, métodos de diagnóstico (rastreamento mamográfico e biópsia), fatores prognósticos, avaliação de biomarcadores (RE, RP, HER2) e opções de tratamento cirúrgico e adjuvante. O objetivo é fornecer uma visão abrangente sobre o CDIS, desde a identificação até as estratégias terapêuticas visando prevenir a progressão para carcinoma invasivo e reduzir o risco de recorrência.
Definição e Características do Carcinoma Ductal In Situ (CDIS)
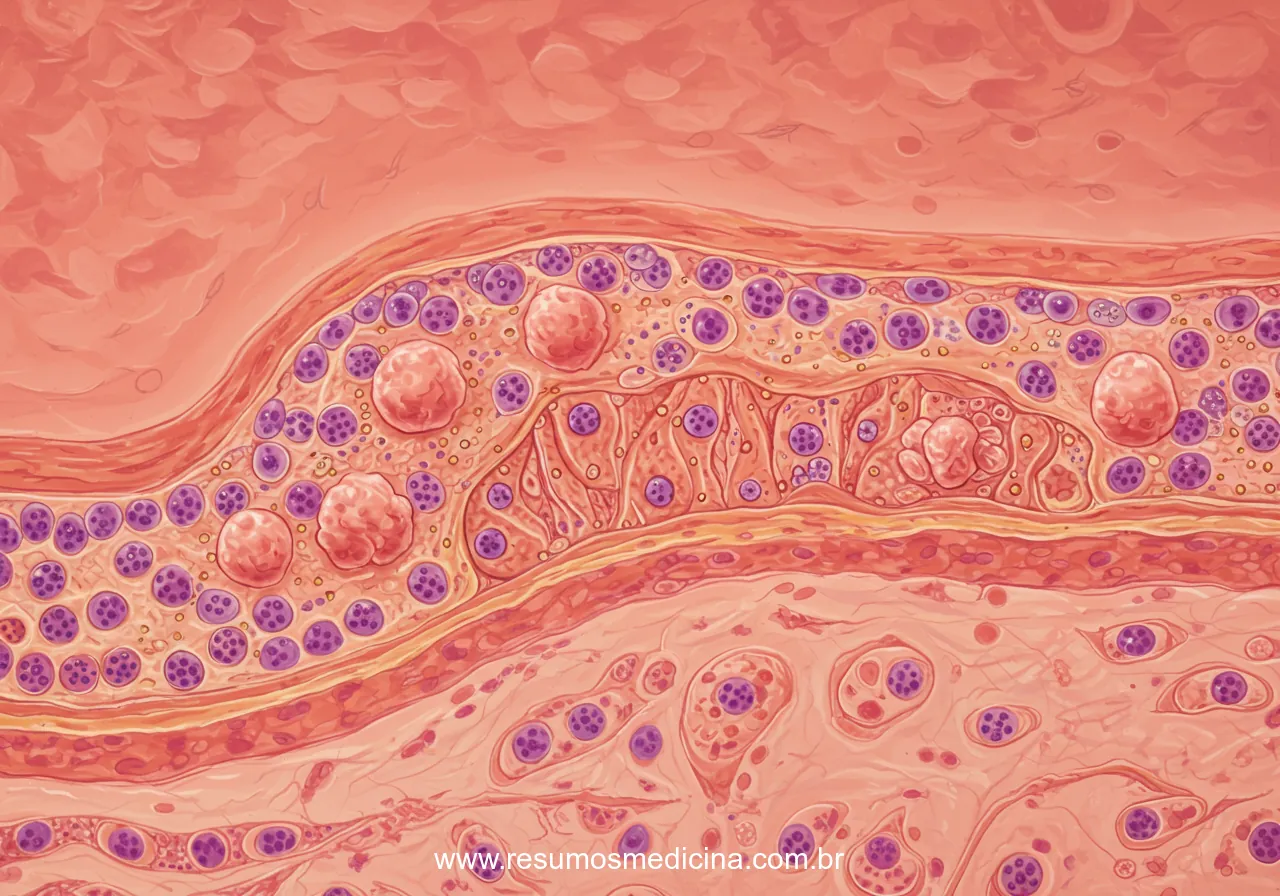
O Carcinoma Ductal In Situ (CDIS) é classificado como uma neoplasia maligna não invasiva da mama, originada a partir da proliferação de células epiteliais anormais ou cancerosas que revestem os ductos mamários. A designação “in situ” sublinha a característica fundamental desta condição: as células neoplásicas estão estritamente confinadas ao interior dos ductos e lóbulos mamários, sem evidência de invasão do estroma circundante. A integridade da membrana basal é preservada, impedindo a disseminação das células para o tecido mamário adjacente.
Características Principais do CDIS
- Natureza Não Invasiva: O critério definidor do CDIS é a ausência de invasão estromal. Diferentemente do carcinoma invasivo, as células malignas no CDIS não romperam a membrana basal dos ductos.
- Lesão Precursora: O CDIS é considerado uma lesão precursora do carcinoma ductal invasivo. Embora não seja imediatamente ameaçador à vida devido à falta de invasão, representa um estágio inicial do câncer de mama com potencial significativo de progressão para doença invasiva se não for adequadamente diagnosticado e tratado.
- Heterogeneidade: O CDIS não é uma entidade única, mas sim um grupo heterogêneo de neoplasias. Apresenta considerável variação em termos de:
- Aparência Histológica: Inclui diferentes padrões arquiteturais como comedo, sólido, cribriforme, papilar e micropapilar.
- Características Citopatológicas: As células podem exibir graus variáveis de pleomorfismo (variação no tamanho e forma) e atipia nuclear (alterações nos núcleos).
- Grau Nuclear: Classificado como baixo, intermediário ou alto, refletindo a agressividade celular.
- Potencial Biológico: Estudos moleculares confirmam uma heterogeneidade substancial, com distintos padrões de expressão gênica entre os subtipos, que podem influenciar o risco de progressão e a resposta terapêutica.
Portanto, o CDIS representa um espectro de alterações malignas não invasivas, confinadas aos ductos mamários. A sua identificação e caracterização precisa, incluindo a avaliação da sua heterogeneidade histopatológica e molecular, são essenciais para determinar o risco de progressão e orientar as estratégias terapêuticas, com o objetivo primário de prevenir a evolução para carcinoma invasivo.
Classificação Histopatológica e Molecular do CDIS
O Carcinoma Ductal In Situ (CDIS) representa um grupo heterogêneo de neoplasias malignas não invasivas, limitadas aos ductos mamários, sem invasão do estroma circundante ou ultrapassagem da membrana basal. Apesar de sua natureza não invasiva, o CDIS é considerado uma lesão precursora do carcinoma invasivo, exibindo variações significativas na aparência histológica, grau nuclear e potencial biológico. A sua classificação é fundamental para a estratificação de risco e orientação terapêutica.
Classificação Histopatológica
A classificação histopatológica tradicional do CDIS baseia-se em características arquiteturais, grau nuclear e presença ou ausência de necrose.
Padrões Arquiteturais
O CDIS é classificado histologicamente com base em seus padrões de crescimento dentro dos ductos. Os principais tipos arquiteturais incluem:
- Comedo: Caracteriza-se pela presença de necrose central extensa dentro dos ductos envolvidos, frequentemente associada a calcificações distróficas detectáveis na mamografia. As células tumorais são tipicamente de alto grau nuclear. Este subtipo é frequentemente associado a um maior risco de recorrência local após excisão cirúrgica incompleta e pode indicar um comportamento mais agressivo.
- Sólido: Os ductos são preenchidos por uma massa sólida de células neoplásicas.
- Cribriforme: Apresenta espaços glandulares secundários, regulares e arredondados dentro da proliferação ductal, conferindo um aspecto fenestrado.
- Papilar: Caracterizado pela formação de estruturas papilares com eixos fibrovasculares dentro dos ductos.
- Micropapilar: Pequenos tufos de células neoplásicas projetam-se para o lúmen ductal, sem eixos fibrovasculares.
É comum a coexistência de múltiplos padrões arquiteturais na mesma lesão. Os subtipos sólido, cribriforme, papilar e micropapilar geralmente estão associados a um menor grau nuclear em comparação com o comedocarcinoma, embora a avaliação prognóstica deva ser individualizada.
Graduação Histológica
A graduação histológica do CDIS é um fator prognóstico crucial, realizada com base no grau nuclear (tamanho, forma e cromaticidade dos núcleos) e na presença ou ausência de necrose. O CDIS é classificado em três graus:
- Baixo Grau (Grau 1): Núcleos pequenos, uniformes, com cromatina fina e nucléolos inconspícuos. Necrose geralmente ausente.
- Grau Intermediário (Grau 2): Características nucleares intermediárias entre baixo e alto grau. Necrose pode estar presente, mas não é extensa como no tipo comedo.
- Alto Grau (Grau 3): Núcleos grandes, pleomórficos (variação de tamanho e forma), com cromatina grosseira e nucléolos proeminentes. Necrose, especialmente do tipo comedo, é frequentemente presente.
O grau nuclear é um dos principais determinantes do grau histológico final. A avaliação pode apresentar desafios relacionados à subjetividade e variabilidade interobservador, destacando a importância da padronização dos critérios.
Classificação Molecular e Biomarcadores
Estudos moleculares revelaram uma considerável heterogeneidade dentro do CDIS, com diferentes subtipos moleculares demonstrando padrões de expressão gênica distintos. Esta heterogeneidade pode refletir diferentes potenciais de progressão e respostas ao tratamento.
A avaliação imuno-histoquímica de biomarcadores é crucial:
- Receptores Hormonais (RE e RP): A expressão de receptores de estrogênio (RE) e progesterona (RP) é frequentemente avaliada. Tumores RE-positivos podem se beneficiar de terapia endócrina adjuvante (Tamoxifeno ou Inibidores da Aromatase) para reduzir o risco de recorrência e desenvolvimento de câncer invasivo.
- HER2 (Receptor 2 do Fator de Crescimento Epidérmico Humano): A avaliação da superexpressão ou amplificação do gene HER2 é importante. Embora as terapias anti-HER2 não sejam padrão no CDIS puro, sua avaliação pode ter implicações prognósticas e ser relevante em contextos específicos ou de pesquisa.
A combinação desses marcadores permite uma classificação molecular complementar, que pode refinar a predição de risco. O subtipo triplo-negativo (RE-, RP-, HER2-), embora menos comum no CDIS, é identificado e pode estar associado a um risco ligeiramente maior de recorrência. É fundamental avaliar a concordância dos biomarcadores entre a biópsia inicial e a peça cirúrgica, devido à possível heterogeneidade tumoral.
Diagnóstico do CDIS: Rastreamento Mamográfico e Biópsia
O diagnóstico do Carcinoma Ductal In Situ (CDIS) frequentemente se inicia no contexto do rastreamento mamográfico. A mamografia é a principal ferramenta para a detecção precoce desta neoplasia não invasiva, sendo responsável por identificar a maioria dos casos, muitos deles em pacientes assintomáticas. O aumento significativo na detecção de CDIS está diretamente relacionado à ampla utilização do rastreamento mamográfico.
Achados Mamográficos Suspeitos
A apresentação radiológica mais comum e característica do CDIS são as microcalcificações. Estas podem exibir morfologias e distribuições variadas, sendo particularmente suspeitas quando se apresentam:
- Pleomórficas: Aparência irregular em forma e tamanho.
- Agrupadas: Concentradas em uma pequena área.
- Lineares ou Ramificadas: Sugerindo preenchimento ductal.
As microcalcificações pleomórficas agrupadas são um achado frequente que levanta forte suspeita de malignidade. No subtipo comedo, a necrose central pode levar à formação de calcificações distróficas, também detectáveis mamograficamente. Embora menos frequentes, outras apresentações como assimetrias focais, distorção arquitetural ou mesmo massas podem indicar a presença de CDIS.
Confirmação Histopatológica por Biópsia
Achados mamográficos suspeitos demandam investigação adicional para confirmação diagnóstica definitiva, que é obtida exclusivamente através da análise histopatológica de uma amostra tecidual. A biópsia é, portanto, um passo essencial.
Diferentes técnicas de biópsia podem ser empregadas:
- Biópsia por Agulha Grossa (Core Biopsy): Frequentemente utilizada, geralmente guiada por imagem (mamografia – estereotaxia, ou ultrassonografia), permite a obtenção de fragmentos teciduais representativos da lesão para análise.
- Mamotomia (Biópsia a Vácuo): Técnica que também permite a coleta de amostras por agulha, frequentemente utilizada para lesões identificadas por calcificações.
- Biópsia Excisional: Remoção cirúrgica de toda a área suspeita, que pode servir tanto para diagnóstico quanto para tratamento inicial em alguns casos.
A análise histopatológica da amostra obtida é crucial. O patologista avalia as características citológicas das células neoplásicas (como grau nuclear, pleomorfismo, atipia), a arquitetura do arranjo celular dentro dos ductos (padrões cribriforme, sólido, papilar, micropapilar, comedo) e a presença ou ausência de necrose. O critério fundamental para o diagnóstico de CDIS é a confirmação da proliferação de células malignas confinadas aos ductos mamários, com a ausência de invasão do estroma circundante, ou seja, a preservação da membrana basal.
Fatores Prognósticos e Avaliação de Biomarcadores (RE, RP, HER2)
A avaliação do Carcinoma Ductal In Situ (CDIS) transcende a simples confirmação diagnóstica, exigindo uma análise detalhada de fatores prognósticos e biomarcadores para estratificar o risco de recorrência e progressão para doença invasiva, bem como orientar as decisões terapêuticas. A heterogeneidade inerente ao CDIS torna essa avaliação individualizada fundamental.
Fatores que Influenciam o Prognóstico
Diversos fatores clínico-patológicos são reconhecidos por influenciarem o prognóstico e o risco associado ao CDIS:
- Grau Nuclear: A graduação histológica, classificada em baixo, intermediário ou alto grau com base principalmente nas características nucleares (tamanho, forma, cromaticidade), é um dos mais importantes fatores prognósticos. O alto grau nuclear reflete maior agressividade celular e está associado a um risco aumentado de recorrência e progressão.
- Presença de Necrose (Comedonecrose): A necrose, especialmente a comedonecrose característica do subtipo comedocarcinoma, é frequentemente associada a tumores de alto grau e indica um maior risco de recorrência local após tratamento conservador.
- Tamanho da Lesão: A extensão da área acometida pelo CDIS é um fator relevante. Lesões maiores podem estar associadas a um maior risco de doença residual após cirurgia e de recorrência subsequente.
- Margens Cirúrgicas: A obtenção de margens cirúrgicas livres de neoplasia após a ressecção é crucial, especialmente na cirurgia conservadora. Margens comprometidas ou exíguas (inferiores a 2mm, embora o ideal seja debatido) aumentam significativamente o risco de recorrência local (como CDIS ou carcinoma invasivo).
- Idade da Paciente: A idade da paciente no momento do diagnóstico também é um fator prognóstico considerado, podendo influenciar o risco de recorrência.
Avaliação Crucial de Biomarcadores: RE, RP e HER2
A análise imuno-histoquímica para determinar o status dos receptores de estrogênio (RE), progesterona (RP) e do receptor 2 do fator de crescimento epidérmico humano (HER2) é um componente essencial na avaliação do CDIS, pois influencia diretamente as opções de tratamento e o prognóstico.
- Receptores Hormonais (RE e RP): A avaliação da expressão de RE e RP é fundamental. Tumores que expressam esses receptores (RE-positivos e/ou RP-positivos) são considerados hormônio-sensíveis. Pacientes com CDIS RE-positivo podem se beneficiar da terapia endócrina adjuvante (com tamoxifeno ou inibidores da aromatase, dependendo do status menopausal), que visa reduzir o risco de recorrência local e o desenvolvimento de novo câncer de mama (invasivo ou in situ). A expressão de receptores hormonais está associada a uma melhor resposta a essa modalidade terapêutica.
- HER2: A avaliação do status do HER2 (superexpressão proteica ou amplificação gênica) também é crucial. A superexpressão de HER2, embora possa ser menos frequente no CDIS puro em comparação com o carcinoma invasivo, impacta as opções terapêuticas e pode indicar um comportamento biológico particular. Sua positividade pode abrir a possibilidade de inclusão em terapias direcionadas anti-HER2, principalmente em cenários de pesquisa clínica ou em casos específicos conforme protocolos institucionais.
Concordância de Biomarcadores entre Biópsia e Peça Cirúrgica
É fundamental considerar a possibilidade de discrepâncias nos resultados dos biomarcadores (RE, RP, HER2) entre a amostra obtida por biópsia inicial (por exemplo, core biopsy) e a peça cirúrgica excisional definitiva. A avaliação da concordância é importante, pois variações podem ocorrer devido à heterogeneidade tumoral intrínseca ou a diferenças nas técnicas de processamento e análise laboratorial. Discrepâncias significativas podem influenciar as decisões terapêuticas subsequentes, reforçando a importância da análise cuidadosa, idealmente na peça cirúrgica, para a definição do tratamento adjuvante.
Significado Clínico do CDIS Triplo-Negativo
O subtipo de CDIS caracterizado pela ausência de expressão de RE, RP e HER2 (triplo-negativo) apresenta características distintas. Embora represente uma minoria dos casos de CDIS, sua identificação é clinicamente importante. O CDIS triplo-negativo pode estar associado a um risco ligeiramente maior de recorrência em comparação com outros subtipos. Além disso, as opções de tratamento sistêmico adjuvante são limitadas para este subtipo, uma vez que não há benefício esperado da terapia endócrina ou da terapia anti-HER2.
Tratamento Cirúrgico: Mastectomia vs. Cirurgia Conservadora e Margens
O tratamento cirúrgico é um componente fundamental na abordagem do Carcinoma Ductal In Situ (CDIS). As principais opções incluem a mastectomia e a cirurgia conservadora da mama (CCM), sendo a escolha entre elas dependente de múltiplos fatores, incluindo a extensão da doença, características do tumor, tamanho da mama e preferências da paciente.
Mastectomia
A mastectomia total é uma opção de tratamento cirúrgico para o CDIS. Suas indicações incluem casos onde a doença é extensa ou multicêntrica, ou quando a cirurgia conservadora não consegue alcançar margens cirúrgicas livres de neoplasia. Em situações que requerem mastectomia, a pesquisa do linfonodo sentinela pode ser considerada, especialmente se houver alta probabilidade de invasão oculta (por exemplo, em CDIS de alto grau ou com extensa necrose).
Cirurgia Conservadora da Mama (CCM)
A cirurgia conservadora, que engloba procedimentos como a tumorectomia, ressecção segmentar ou quadrantectomia, representa uma alternativa à mastectomia para mulheres com doença menos extensa e que almejam a preservação da mama. Esta abordagem é particularmente aplicável a lesões menores e bem localizadas. A viabilidade da CCM está condicionada à possibilidade de ressecar completamente a lesão, obtendo margens cirúrgicas livres de células neoplásicas, mantendo um resultado estético aceitável.
A Importância Crucial das Margens Cirúrgicas na CCM
Na cirurgia conservadora do CDIS, a obtenção de margens cirúrgicas livres de doença é de importância crucial. Margens negativas (sem células neoplásicas na borda da amostra cirúrgica ressecada) são fundamentais para minimizar o risco de recorrência local da doença, seja como CDIS ou como carcinoma invasivo. Fatores como margens cirúrgicas insuficientes aumentam significativamente este risco.
Embora a extensão ideal da margem livre seja um ponto de discussão na literatura, margens mais amplas estão associadas a menores taxas de recorrência local. Uma recomendação comum, baseada em consensos e diretrizes, é a obtenção de margens de, no mínimo, 2mm. A avaliação precisa das margens é realizada pelo patologista no exame histopatológico da peça cirúrgica.
A decisão final sobre a abordagem cirúrgica (mastectomia vs. CCM) e a gestão das margens deve ser individualizada, considerando as características específicas do CDIS (tamanho, grau, localização, multicentricidade), a capacidade técnica de obter margens adequadas e as preferências informadas da paciente.
Terapias Adjuvantes: Radioterapia e Hormonioterapia
Após o tratamento cirúrgico primário do Carcinoma Ductal In Situ (CDIS), terapias adjuvantes como a radioterapia e a hormonioterapia desempenham um papel crucial na redução do risco de recorrência da doença e na prevenção da progressão para carcinoma invasivo.
Radioterapia Adjuvante
A radioterapia adjuvante é frequentemente recomendada após a cirurgia conservadora (tumorectomia, ressecção segmentar ou setorectomia) para o CDIS. O principal objetivo desta abordagem é eliminar possíveis células tumorais residuais, reduzindo significativamente o risco de recorrência local, tanto na forma de CDIS quanto de carcinoma invasivo. A indicação para radioterapia é particularmente relevante em casos considerados de maior risco, como aqueles com margens cirúrgicas comprometidas ou próximas, tumores de alto grau histológico, ou em pacientes com outros fatores de risco adicionais, como a idade. A decisão de utilizar a radioterapia deve ponderar seus benefícios na redução da recorrência local frente aos potenciais efeitos colaterais a longo prazo, conforme descrito em diversas fontes.
Hormonioterapia (Terapia Endócrina)
A hormonioterapia adjuvante, também referida como terapia endócrina, é uma estratégia terapêutica indicada especificamente para pacientes com CDIS cujos tumores expressam receptores hormonais positivos (RE+ e/ou RP+). O objetivo é reduzir o risco de recorrência e o desenvolvimento subsequente de câncer invasivo. Esta terapia atua bloqueando os efeitos do estrogênio sobre as células tumorais.
Os principais agentes utilizados são:
- Tamoxifeno: Pode ser utilizado em mulheres tanto na pré-menopausa quanto na pós-menopausa.
- Inibidores da Aromatase (IA): São tipicamente utilizados apenas em mulheres na pós-menopausa. Sua ação se baseia na inibição da produção periférica de estrogênio, não influenciando a produção ovariana, que é a principal fonte de estrogênio em mulheres na pré-menopausa.
A escolha do agente específico e a duração da terapia endócrina dependem fundamentalmente do status menopausal da paciente e das características clínico-patológicas do tumor.
Biópsia do Linfonodo Sentinela (BLS) e Risco de Recorrência
A abordagem do Carcinoma Ductal In Situ (CDIS) envolve considerações específicas quanto ao estadiamento axilar e ao potencial de recorrência pós-tratamento. A Biópsia do Linfonodo Sentinela (BLS), um procedimento padrão na avaliação de carcinomas invasivos, não é indicada de rotina no contexto do CDIS puro. Isso se fundamenta na natureza não invasiva da lesão, que está confinada aos ductos mamários e, teoricamente, não apresenta capacidade de disseminação linfática.
No entanto, existem situações clínicas específicas em que a BLS pode ser considerada no manejo do CDIS:
- Planejamento de Mastectomia: A realização de mastectomia para tratamento do CDIS é uma indicação para BLS. A remoção completa da mama impossibilita a realização futura da BLS caso um foco de invasão oculto seja identificado na peça cirúrgica final.
- Alta Suspeita de Invasão ou Microinvasão: Casos de CDIS com características que elevam a probabilidade de invasão subjacente, como lesões de alto grau nuclear, presença de extensa necrose (padrão comedo), ou achados suspeitos de microinvasão na biópsia inicial ou excisional, podem justificar a BLS.
O objetivo da BLS nessas circunstâncias é identificar precocemente a disseminação para os linfonodos axilares, o que alteraria significativamente o estadiamento da doença e o plano terapêutico subsequente.
Risco de Recorrência Após Tratamento
Apesar do prognóstico geralmente favorável do CDIS, existe um risco inerente de recorrência local após o tratamento, que pode se manifestar tanto como um novo evento de CDIS quanto como um carcinoma invasivo. A compreensão dos fatores associados a esse risco é crucial para o planejamento terapêutico e o seguimento adequado.
Diversos fatores prognósticos influenciam a probabilidade de recorrência local:
- Status das Margens Cirúrgicas: A obtenção de margens cirúrgicas livres de neoplasia é fundamental, especialmente no tratamento conservador (tumorectomia). Margens insuficientes, próximas ou comprometidas aumentam significativamente o risco de recidiva.
- Grau Histológico: O CDIS de alto grau nuclear está associado a um maior risco de recorrência local em comparação com lesões de baixo ou intermediário grau.
- Presença de Necrose (Comedonecrose): A identificação de comedonecrose no exame histopatológico também é um fator associado a um maior risco de recorrência.
- Ausência de Radioterapia Adjuvante: Após a cirurgia conservadora, a omissão da radioterapia adjuvante é um dos principais fatores de risco para recorrência local, particularmente em pacientes com CDIS de alto grau, margens comprometidas ou doença extensa. A radioterapia visa erradicar células neoplásicas residuais, reduzindo a probabilidade de recidiva.
- Outros Fatores: Tamanho da lesão, subtipo histológico e características moleculares (como status de receptores hormonais e HER2) também podem influenciar o prognóstico e o risco de recorrência.
O seguimento cuidadoso com exames clínicos e mamografia é essencial para a detecção precoce de eventuais recorrências, permitindo intervenções oportunas.
Conclusão
O Carcinoma Ductal In Situ (CDIS) apresenta-se como uma condição complexa e heterogênea, exigindo uma abordagem multidisciplinar que englobe desde o diagnóstico preciso até a definição de estratégias terapêuticas individualizadas. A classificação histopatológica e molecular, a avaliação de fatores prognósticos e biomarcadores, e a escolha do tratamento cirúrgico e adjuvante mais adequados são etapas cruciais para otimizar os resultados e minimizar o risco de recorrência e progressão para carcinoma invasivo. A identificação precoce através do rastreamento mamográfico, seguida da confirmação por biópsia e da análise detalhada das características tumorais, possibilita a implementação de intervenções oportunas e eficazes. O seguimento contínuo e a atenção às particularidades de cada caso são, portanto, essenciais para garantir o melhor prognóstico e a qualidade de vida das pacientes diagnosticadas com CDIS.